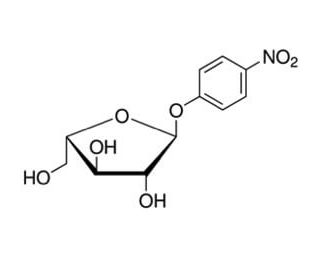
Molekülstruktur von 4-Nitrophenyl α-L-arabinofuranoside, CAS-Nummer: 6892-58-6
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6)
Produktreferenzen ansehen (1)
Alternative Namen:
pNP-alpha-L-Arabinofuranoside
CAS Nummer:
6892-58-6
Reinheit:
≥98%
Molekulargewicht:
271.22
Summenformel:
C11H13NO7
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Publikationen
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
4-Nitrophenyl-α-L-arabinofuranosid ist eine synthetische Verbindung, die in der Biochemie und Molekularbiologie häufig als chromogenes Substrat für die Bestimmung der α-L-Arabinofuranosidase-Aktivität verwendet wird. α-L-Arabinofuranosidasen sind Enzyme, die die Hydrolyse von α-L-Arabinofuranosid-Bindungen katalysieren, die in verschiedenen natürlichen Verbindungen, einschließlich Polysacchariden und Glykokonjugaten, vorkommen. Diese Enzyme spielen eine Rolle beim Abbau und Stoffwechsel komplexer Kohlenhydrate und tragen zum Abbau pflanzlicher Biomasse und zum Kreislauf der organischen Materie in der Umwelt bei.
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6) Literaturhinweise
- Bifunktionelle Glykosidhydrolasen der Familie 3 aus Gerste mit alpha-L-Arabinofuranosidase- und beta-D-Xylosidase-Aktivität. Charakterisierung, Primärstrukturen und COOH-terminale Verarbeitung. | Lee, RC., et al. 2003. J Biol Chem. 278: 5377-87. PMID: 12464603
- Die Acetate von p-Nitrophenyl-alpha-L-arabinofuranosid-regioselektive Herstellung durch Einwirkung von Lipasen. | Mastihubová, M., et al. 2006. Bioorg Med Chem. 14: 1805-10. PMID: 16288881
- Variation der relativen Substratspezifität von bifunktioneller beta-D-Xylosidase/alpha-L-Arabinofuranosidase durch Mutationen an einer Stelle: Rolle der Substratverzerrung und -erkennung. | Jordan, DB. and Li, XL. 2007. Biochim Biophys Acta. 1774: 1192-8. PMID: 17689155
- Konstruktion und Charakterisierung von zwei chimären Xylan abbauenden Enzymen. | Fan, Z., et al. 2009. Biotechnol Bioeng. 102: 684-92. PMID: 18828173
- Thermodynamik der Hydrolysereaktionen von 1-Naphthylacetat, 4-Nitrophenylacetat und 4-Nitrophenyl-α-L-arabinofuranosid. | Decker, SR., et al. 2010. J Phys Chem B. 114: 16060-7. PMID: 20361764
- Neuartige bifunktionelle alpha-L-Arabinofuranosidase/xylobiohydrolase (ABF3) aus Penicillium purpurogenum. | Ravanal, MC., et al. 2010. Appl Environ Microbiol. 76: 5247-53. PMID: 20562284
- Wirkung von Xylan deacetylierenden Enzymen auf Monoacetylderivate von 4-Nitrophenylglycosiden von β-D-Xylopyranose und α-L-Arabinofuranose. | Biely, P., et al. 2011. J Biotechnol. 151: 137-42. PMID: 21029756
- Reinigung und Charakterisierung von Arabinofuranosidase aus dem Mais-Endophyten Acremonium zeae. | Bischoff, KM., et al. 2011. Biotechnol Lett. 33: 2013-8. PMID: 21671092
- Die Analyse der Arabinoxylan-Arabinofuranohydrolase-Genfamilie in Gerste belegt nicht ihre Beteiligung am Umbau der Endospermzellwände während der Entwicklung. | Laidlaw, HK., et al. 2012. J Exp Bot. 63: 3031-45. PMID: 22378943
- Aktivierung einer GH43 β-Xylosidase durch zweiwertige Metalle. | Lee, CC., et al. 2013. Enzyme Microb Technol. 52: 84-90. PMID: 23273276
- Eine neuartige bifunktionelle GH51 exo-α-l-Arabinofuranosidase/endo-xylanase aus Alicyclobacillus sp. A4 mit signifikanter Biomasseabbaukapazität. | Yang, W., et al. 2015. Biotechnol Biofuels. 8: 197. PMID: 26628911
- Charakterisierung einer mutmaßlichen Arabinofuranosidase der Glycosidhydrolase-Familie 43 aus Aspergillus niger und ihre mögliche Verwendung bei der Bierherstellung. | Li, X., et al. 2020. Food Chem. 305: 125382. PMID: 31525590
- Charakterisierung und Funktionsanalyse von zwei neuen thermotoleranten α-L-Arabinofuranosidasen, die zur Glycosidhydrolase-Familie 51 aus Thielavia terrestris und zur Familie 62 aus Eupenicillium parvum gehören. | Long, L., et al. 2020. Appl Microbiol Biotechnol. 104: 8719-8733. PMID: 32880690
- Die Beta-D-Xylosidase von Trichoderma reesei ist eine multifunktionelle Beta-D-Xylan-Xylohydrolase. | Herrmann, MC., et al. 1997. Biochem J. 321 (Pt 2): 375-81. PMID: 9020869
- Reinigung und Charakterisierung einer neuartigen thermostabilen alpha-L-Arabinofuranosidase aus einem farblich variierenden Stamm von Aureobasidium pullulans. | Saha, BC. and Bothast, RJ. 1998. Appl Environ Microbiol. 64: 216-20. PMID: 9435077
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-Nitrophenyl α-L-arabinofuranoside, 10 mg | sc-220982 | 10 mg | $109.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 25 mg | sc-220982A | 25 mg | $203.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 50 mg | sc-220982B | 50 mg | $359.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 100 mg | sc-220982C | 100 mg | $515.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 250 mg | sc-220982D | 250 mg | $983.00 |
