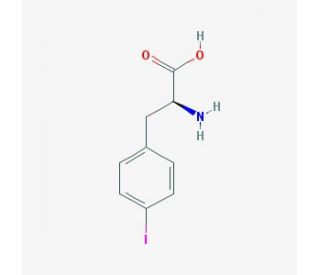
Molekülstruktur von 4-Iodo-L-phenylalanine, CAS-Nummer: 24250-85-9
4-Iodo-L-phenylalanine (CAS 24250-85-9)
Alternative Namen:
p-Iodo-L-phenylalanine
Anwendungen:
4-Iodo-L-phenylalanine wird in der Proteinentwicklung als Modell für eine unnatürliche α-Aminosäure verwendet, um die primäre Aminosäurezusammensetzung über das Opal-Codon (UGA) zu verändern.
CAS Nummer:
24250-85-9
Reinheit:
≥98%
Molekulargewicht:
291.10
Summenformel:
C9H10INO2
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
4-Iodo-L-Phenylalanin kann in der Protein-Engineering als eine unnatürliche Alpha-Aminosäure verwendet werden, um die primäre Aminosäure-Zusammensetzung mithilfe des Opal (UGA)-Codons zu verändern. Die Anwesenheit von 4-Iodo-L-Phenylalanin hemmt die Translation, indem es während des Translationsprozesses mit dem Ribosom interagiert. Darüber hinaus bindet es an die Hydroxylgruppe einer mRNA-Molekül während der Transkription. Als Ergebnis dieser Hemmung kommt es zu einer Abnahme der Protein-Synthese und der Proliferation von Zellen.
4-Iodo-L-phenylalanine (CAS 24250-85-9) Literaturhinweise
- p-Ethinylphenylalanin: ein starker Inhibitor der Tryptophanhydroxylase. | Stokes, AH., et al. 2000. J Neurochem. 74: 2067-73. PMID: 10800950
- Regioselektive Kohlenstoff-Kohlenstoff-Bindungsbildung in Proteinen mit Palladiumkatalyse; neue Proteinchemie durch metallorganische Chemie. | Kodama, K., et al. 2006. Chembiochem. 7: 134-9. PMID: 16307466
- Ein neuer Ansatz für das Protein-Engineering, der Chemie und Biologie kombiniert, Teil I: ortsspezifischer Einbau von 4-Jod-L-Phenylalanin in vitro unter Verwendung von misacyliertem Suppressor tRNAPhe. | Kodama, K., et al. 2006. Chembiochem. 7: 1577-81. PMID: 16969782
- Ortsspezifische Funktionalisierung von Proteinen durch Organopalladiumreaktionen. | Kodama, K., et al. 2007. Chembiochem. 8: 232-8. PMID: 17195252
- Ortsspezifischer Einbau von 4-Jod-L-Phenylalanin durch Opal-Suppression. | Kodama, K., et al. 2010. J Biochem. 148: 179-87. PMID: 20495012
- Unterscheidung von enantiomeren Arzneimitteln durch jodsubstituierte L-Aminosäure-Referenzen unter massenspektrometrischen Elektrospray-Ionisierungsbedingungen. | Karthikraj, R., et al. 2012. Rapid Commun Mass Spectrom. 26: 1385-91. PMID: 22555933
- Enantiomerendifferenzierung von β-Aminoalkoholen unter elektrosprayionisationsmassenspektrometrischen Bedingungen. | Karthikraj, R., et al. 2014. J Mass Spectrom. 49: 108-16. PMID: 24446270
- Röntgendichte, jodfunktionalisierte, auf Phenylalanin basierende Poly(esterharnstoffe). | Li, S., et al. 2015. Biomacromolecules. 16: 615-24. PMID: 25575022
- Ortsspezifische Spin-Markierung von Proteinen durch Suzuki-Miyaura-Kopplung über eine genetisch kodierte Aryliodid-Aminosäure. | Kugele, A., et al. 2019. Chem Commun (Camb). 55: 1923-1926. PMID: 30680379
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-Iodo-L-phenylalanine, 1 g | sc-216895 | 1 g | $143.00 | |||
4-Iodo-L-phenylalanine, 5 g | sc-216895A | 5 g | $275.00 | |||
4-Iodo-L-phenylalanine, 25 g | sc-216895B | 25 g | $541.00 |
