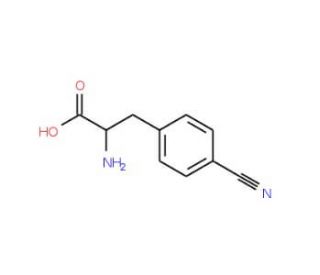
4-Cyano-L-phenylalanine (CAS 104531-20-6)
Direktverknüpfungen
4-Cyano-L-Phenylalanin ist ein Aminosäurederivat und gehört zur Klasse der aromatischen Aminosäuren. 4-Cyano-L-Phenylalanin ist durch das Vorhandensein einer Cyano (CN)-Gruppe, die an das Phenylalanin-Molekül gebunden ist, charakterisiert. In der wissenschaftlichen Forschung findet 4-Cyano-L-Phenylalanin aufgrund seiner einzigartigen chemischen Eigenschaften verschiedene Anwendungen. Es wird häufig als Baustein oder Vorläufer in der Peptidsynthese und der Arzneimittelforschung verwendet. Die Cyano-Gruppe kann als vielseitige Funktionsgruppe dienen und ermöglicht die Einführung vielfältiger chemischer Modifikationen und die Erstellung von Peptidanaloga mit veränderten biologischen Aktivitäten. Eine der wichtigsten Anwendungen von 4-Cyano-L-Phenylalanin ist das Gebiet der Medizinischen Chemie. Forscher nutzen diese Verbindung, um neue Peptide mit erhöhter Bioaktivität, Stabilität oder pharmakokinetischen Eigenschaften zu entwickeln. Durch die Einbindung von 4-Cyano-L-Phenylalanin in Peptidsequenzen können Wissenschaftler die Wechselwirkungen des Peptids mit biologischen Zielen wie Rezeptoren oder Enzymen modulieren, was möglicherweise zu einer verbesserten therapeutischen Wirksamkeit führt. Der Wirkmechanismus von 4-Cyano-L-Phenylalanin hängt vom spezifischen Kontext und dem Peptid oder Molekül ab, in das es eingebunden ist. Als Aminosäurederivat kann 4-Cyano-L-Phenylalanin an der Peptidbindungsbildung während der Synthese teilnehmen und zur Gesamtstruktur und Funktion des resultierenden Peptids beitragen. Die Anwesenheit der Cyano-Gruppe kann die Wechselwirkungen des Peptids mit biologischen Zielen durch Veränderung seiner Konformation, Stabilität oder Rezeptorbindungsaffinität beeinflussen. Darüber hinaus kann die Cyano-Gruppe chemische Reaktionen durchlaufen, was weitere Modifikationen oder Funktionalisierungen des Peptids ermöglicht. Diese Modifikationen können die Löslichkeit des Peptids, die Membranpermeabilität oder die metabolische Stabilität beeinflussen und somit sein Verhalten in biologischen Systemen beeinflussen.
4-Cyano-L-phenylalanine (CAS 104531-20-6) Literaturhinweise
- Neue chromogene Substrate von humanem neutrophilem Cathepsin G, die nicht natürliche aromatische Aminosäurereste in Position P(1) enthalten, ausgewählt durch Methoden der kombinatorischen Chemie. | Wysocka, M., et al. 2007. Mol Divers. 11: 93-9. PMID: 17653609
- Erweiterung des Nutzens von 4-Cyano-L-Phenylalanin als Schwingungsreporter von Proteinumgebungen. | Bazewicz, CG., et al. 2012. J Phys Chem B. 116: 10824-31. PMID: 22909326
- Rationales Design eines Zink-Phthalocyanin-bindenden Proteins. | Mutter, AC., et al. 2014. J Struct Biol. 185: 178-85. PMID: 23827257
- Empfindliche, ortsspezifische und stabile Schwingungssonde für lokale Proteinumgebungen: 4-Azidomethyl-L-phenylalanin. | Bazewicz, CG., et al. 2013. J Phys Chem B. 117: 8987-93. PMID: 23865850
- Die 'Torwächter'-Rolle von Trp222 bestimmt die Enantiopräferenz der Diketoreduktase gegenüber 2-Chlor-1-phenylethanon. | Ma, H., et al. 2014. PLoS One. 9: e103792. PMID: 25072248
- Isolierung und synthetische Diversifizierung von Jadomycin 4-Amino-l-phenylalanin. | Martinez-Farina, CF., et al. 2015. J Nat Prod. 78: 1208-14. PMID: 26035093
- Verbesserter Einbau von nicht-kanonischen Aminosäuren durch einen manipulierten tRNA(Tyr)-Suppressor. | Rauch, BJ., et al. 2016. Biochemistry. 55: 618-28. PMID: 26694948
- Untersuchung der Wirksamkeit des spektroskopischen Reporters für unnatürliche Aminosäuren: eine Strukturstudie. | Dippel, AB., et al. 2016. Acta Crystallogr D Struct Biol. 72: 121-30. PMID: 26894540
- Vergleich biologischer Chromophore: photophysikalische Eigenschaften von Cyanophenylalanin-Derivaten. | Martin, JP., et al. 2016. Phys Chem Chem Phys. 18: 20750-7. PMID: 27412819
- Minimalistische IR- und Fluoreszenzsonden für Proteinfunktionen. | Gosavi, PM. and Korendovych, IV. 2016. Curr Opin Chem Biol. 34: 103-109. PMID: 27599185
- Untersuchung lokaler Solvatationsumgebungen eines Häm-Proteins mit Hilfe des spektroskopischen Reporters 4-Cyano-l-Phenylalanin. | Kearney, C., et al. 2018. RSC Adv. 8: 13503-13512. PMID: 29780583
- Kristallstrukturen von grün fluoreszierendem Protein mit der unnatürlichen Aminosäure 4-Nitro-L-Phenylalanin. | Maurici, N., et al. 2018. Acta Crystallogr F Struct Biol Commun. 74: 650-655. PMID: 30279317
- Strukturelle und spektrophotometrische Untersuchung von zwei unnatürlichen, durch Aminosäuren veränderten Chromophoren im grün fluoreszierenden Superfolder-Protein. | Olenginski, GM., et al. 2021. Acta Crystallogr D Struct Biol. 77: 1010-1018. PMID: 34342274
- Neu entwickelte Peptide für die zelluläre Abgabe und subzelluläre Lokalisierung. | Rhys, GG., et al. 2022. Nat Chem Biol. 18: 999-1004. PMID: 35836017
- Entschlüsselung komplexer lokaler Proteinumgebungen mit 4-Cyano-l-Phenylalanin. | Lee, B., et al. 2022. J Phys Chem B. 126: 8957-8969. PMID: 36317866
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-Cyano-L-phenylalanine, 1 g | sc-290253 | 1 g | $156.00 | |||
4-Cyano-L-phenylalanine, 5 g | sc-290253A | 5 g | $604.00 |
