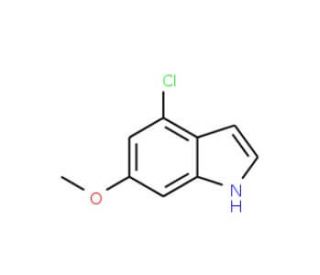
4-Chloro-6-methoxy Indole (CAS 93490-31-4)
Direktverknüpfungen
4-Chlor-6-methoxy-Indol wird wegen seiner Rolle als Zwischenprodukt bei der Synthese einer Vielzahl komplexer organischer Moleküle aktiv untersucht. Es ist ein Schlüsselreagenz auf dem Gebiet der organischen Synthese, wo Forscher seine Reaktivität bei verschiedenen chemischen Umwandlungen untersuchen. Von besonderem Interesse ist der Nutzen der Verbindung bei katalytischen Reaktionen, da sie häufig an der Bildung neuer Bindungen durch Kreuzkupplungsreaktionen beteiligt ist. In der Materialwissenschaft wird 4-Chlor-6-methoxy-Indol aufgrund seiner Indolstruktur, die zu den gewünschten elektronischen Eigenschaften beitragen kann, auf seine mögliche Einbindung in organische elektronische Materialien untersucht. Darüber hinaus wird es bei der Entdeckung neuer Liganden für Übergangsmetallkatalysatoren eingesetzt, was zur Entwicklung effizienterer und selektiverer Synthesewege beiträgt. Die Rolle der Verbindung bei der Synthese von Naturstoffen und deren Analoga ist ein weiterer wichtiger Anwendungsbereich, der den Fortschritt in der organischen Chemie und verwandten Disziplinen fördert.
4-Chloro-6-methoxy Indole (CAS 93490-31-4) Literaturhinweise
- Mutagene Aktivitäten von Tryptophan-Metaboliten vor und nach der Behandlung mit Nitrit. | Hashizume, T., et al. 1991. Food Chem Toxicol. 29: 839-44. PMID: 1765329
- In-vitro-Tests und das karzinogene Potenzial verschiedener nitrosierter Indolverbindungen. | Tiedink, HG., et al. 1991. Cell Biol Toxicol. 7: 371-86. PMID: 1794111
- Die Stabilität der nitrosierten Produkte von Indol, Indol-3-acetonitril, Indol-3-carbinol und 4-Chlorindol. | Tiedink, HG., et al. 1989. Food Chem Toxicol. 27: 723-30. PMID: 2693284
- 32P-Postlabeling-Analyse von DNA-Addukten im Rattenmagen mit 1-Nitrosoindol-3-acetonitril, einer direkt wirkenden mutagenen Indolverbindung, die durch Nitrosierung gebildet wird. | Yamashita, K., et al. 1988. Carcinogenesis. 9: 1905-7. PMID: 3168167
- Alkylierende Aktivität in Lebensmitteln - insbesondere in Sauerkraut und sauer vergorenen Milchprodukten - nach Inkubation mit Nitrit unter quasi-gastrischen Bedingungen. | Groenen, PJ. and Busink, E. 1988. Food Chem Toxicol. 26: 215-25. PMID: 3366423
- Induktion von Mundhöhlenkrebs durch 3-Diazotyramin, ein Nitrosierungsprodukt von Tyramin in Lebensmitteln. | Fujita, Y., et al. 1987. Carcinogenesis. 8: 527-9. PMID: 3829319
- 4-Chlor-6-methoxyindol ist der Vorläufer eines starken Mutagens (4-Chlor-6-methoxy-2-hydroxy-1-nitroso-indolin-3-one oxime), das bei der Nitrosierung der Favabohne (Vicia faba) entsteht. | Yang, D., et al. 1984. Carcinogenesis. 5: 1219-24. PMID: 6548421
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-Chloro-6-methoxy Indole, 10 mg | sc-210003 | 10 mg | $380.00 |
