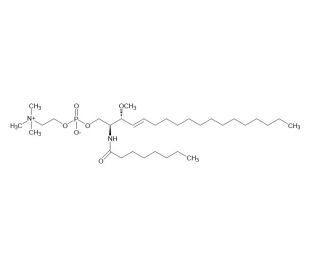
3-O-Methylsphingomyelin
Vedere citazioni di prodotto (1)
LINK RAPIDI
La 3-O-metilsfingomielina è una forma modificata di sfingomielina, un tipo di sfingolipide presente nelle membrane delle cellule animali. La sfingomielina è un componente importante della guaina mielinica, che isola gli assoni e consente una trasmissione efficiente dei segnali elettrici nei neuroni. Si trova anche in vari altri tipi di cellule e ha un ruolo nella segnalazione cellulare e nell'apoptosi. La 3-O-metilsfingomielina è un nuovo inibitore selettivo della N-SMasi (sfingomielinasi neutra), (Ki=37 muM) che è permeabile alle cellule e non inibisce la sfingomielinasi acida. La N-SMasi è un enzima responsabile dell'idrolizzazione della sfingomielina in ceramide e fosforilcolina. La ceramide è un lipide bioattivo coinvolto in una serie di processi cellulari, tra cui l'arresto del ciclo cellulare, l'apoptosi e l'infiammazione. Inibendo selettivamente la N-SMasi e non la sfingomielinasi acida, la 3-O-metilsfingomielina offre una modulazione mirata del metabolismo degli sfingolipidi.
3-O-Methylsphingomyelin Referenze
- Il ruolo della ceramide prodotta dalla sfingomielinasi neutra nell'espressione mediata dal lipopolisaccaride dell'ossido nitrico sintasi inducibile. | Won, JS., et al. 2004. J Neurochem. 88: 583-93. PMID: 14720208
- Le sfingomieline sopprimono la distruzione mirata dei lisosomi/endosomi da parte del fotosensibilizzatore NPe6 durante la terapia fotodinamica. | Caruso, JA., et al. 2005. Biochem J. 392: 325-34. PMID: 15943580
- Modulazione del recettore degli idrocarburi arilici dell'apoptosi indotta dal fattore di necrosi tumorale alfa e della distruzione lisosomiale in un modello di epatoma indipendente dalla caspasi-8. | Caruso, JA., et al. 2006. J Biol Chem. 281: 10954-67. PMID: 16446372
- L'espressione di iNOS indotta da IL-1beta, il rilascio di NO e la perdita di vitalità metabolica delle cellule sono resistenti agli inibitori della ceramide sintasi e della sfingomielinasi nelle cellule INS 832/13. | Veluthakal, R., et al. 2006. JOP. 7: 593-601. PMID: 17095838
- La generazione de novo di C16 e C24-ceramide contribuisce all'apoptosi spontanea dei neutrofili. | Seumois, G., et al. 2007. J Leukoc Biol. 81: 1477-86. PMID: 17329567
- Una nuova via non trascrizionale media gli effetti proconvulsivi dell'interleuchina-1beta. | Balosso, S., et al. 2008. Brain. 131: 3256-65. PMID: 18952671
- L'atrofia muscolare scheletrica indotta da TNF-α e tumori coinvolge il metabolismo degli sfingolipidi. | De Larichaudy, J., et al. 2012. Skelet Muscle. 2: 2. PMID: 22257771
- L'interleuchina-1β endogena nei ratti neuropatici aumenta il rilascio di glutammato dalle afferenze primarie del corno dorsale spinale attraverso l'accoppiamento con i recettori presinaptici dell'acido N-metil-D-aspartico. | Yan, X., et al. 2013. J Biol Chem. 288: 30544-30557. PMID: 24003233
- Il gruppo box-1 ad alta mobilità contenente disolfuro promuove la funzione del recettore N-metil-D-aspartato e l'eccitotossicità attivando la segnalazione dipendente dal recettore Toll-like 4 nei neuroni dell'ippocampo. | Balosso, S., et al. 2014. Antioxid Redox Signal. 21: 1726-40. PMID: 24094148
- Nuovo glicoside oleilico come agente antitumorale che ha come bersaglio la sfingomielinasi neutra. | Romero-Ramírez, L., et al. 2015. Biochem Pharmacol. 97: 158-72. PMID: 26206186
- L'omeostasi della zattera lipidica di membrana è direttamente collegata alla neurodegenerazione. | Moll, T., et al. 2021. Essays Biochem. 65: 999-1011. PMID: 34623437
- La senescenza delle cellule muscolari lisce vascolari accelera l'aggregazione della medina attraverso la secrezione di piccole vescicole extracellulari e la riorganizzazione della matrice extracellulare. | Whitehead, M., et al. 2023. Aging Cell. 22: e13746. PMID: 36433666
- Mutazione di delezione multi-locus indotta da nanoparticelle d'argento: Ruolo della disfunzione lisosomale-autofagia. | Si, B., et al. 2023. Ecotoxicol Environ Saf. 257: 114947. PMID: 37105094
- Interazione della sfingomielinasi con analoghi della sfingomielina modificati nelle posizioni C-1 e C-3 della spina dorsale della sfingosina. | Lister, MD., et al. 1995. Biochim Biophys Acta. 1256: 25-30. PMID: 7742352
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
3-O-Methylsphingomyelin, 1 mg | sc-205580 | 1 mg | $126.00 | |||
3-O-Methylsphingomyelin, 5 mg | sc-205580A | 5 mg | $520.00 |
