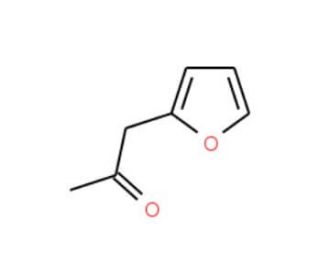
2-Furylacetone (CAS 6975-60-6)
Direktverknüpfungen
2-Furylacetone ist eine Verbindung, die natürlich vorkommt und in Spuren in den ätherischen Ölen von Pflanzen wie Ingwer, Muskatnuss und Nelke gefunden werden kann. Forscher untersuchen 2-Furylacetone aufgrund seiner Fähigkeit, mit bestimmten Enzymen zu interagieren und diese zu hemmen, wie zum Beispiel Cyclooxygenase-2 (COX-2), das eine Rolle bei der Bildung von entzündlichen Mediatoren wie Prostaglandinen spielt. Darüber hinaus wurde festgestellt, dass 2-Furylacetone die Funktion des Enzyms Acetylcholinesterase behindert, das für den Abbau des Neurotransmitters Acetylcholin verantwortlich ist. Die Hemmung dieses Enzyms führt zu einem Anstieg der Acetylcholin-Spiegel, was mit einer verbesserten kognitiven Funktion in Verbindung gebracht wurde.
2-Furylacetone (CAS 6975-60-6) Literaturhinweise
- Aryltriflate: nützliche Kupplungspartner für die direkte Arylierung von Heteroarylderivaten über Pd-katalysierte C-H-Aktivierungsfunktionalisierung. | Roger, J. and Doucet, H. 2008. Org Biomol Chem. 6: 169-74. PMID: 18075663
- Katalytische enantioselektive Reformatsky-Reaktion mit Ketonen. | Fernández-Ibáñez, MA., et al. 2008. Chem Commun (Camb). 2571-3. PMID: 18506247
- Enantioselektive Friedel-Crafts-Alkylierungen von Furanen durch HOMO-Aktivierung. | Li, JL., et al. 2014. Angew Chem Int Ed Engl. 53: 5449-52. PMID: 24756964
- Verbesserung einer Headspace-Mikroextraktions-Gaschromatographie/Massenspektrometrie-Methode für die Analyse von flüchtigen Verbindungen in Weizenbrot. | Raffo, A., et al. 2015. J Chromatogr A. 1406: 266-78. PMID: 26118802
- α,α-Dicyanoolefine: vielseitige Substrate in organokatalytischen asymmetrischen Transformationen. | Kaur, J., et al. 2016. Org Biomol Chem. 14: 7832-47. PMID: 27405916
- Brechung der Aromatizität mit Aminokatalyse: Eine bequeme Strategie für die asymmetrische Synthese. | Przydacz, A., et al. 2019. Angew Chem Int Ed Engl. 58: 63-73. PMID: 30126029
- Höhere Ölausbeute und Qualität von ätherischem Öl aus Aquilaria malaccensis-Holz mit der subkritischen Technik. | Samadi, M., et al. 2020. Molecules. 25: PMID: 32858782
- Furyl- und Tetrahydrofuryl-alkylamine | WALTER C. McCARTHY and RAYMOND J. KAHL. 1956. J. Org. Chem. 21, 10: 1118–1119.
- Die Ultraviolett-Absorptionsspektren bestimmter Arylketone, vor allem Benzylacetone | Samuel F. Marsocci and Scott MacKenzie. 1959. J. Am. Chem. Soc. 81, 17: 4513–4516.
- Flüchtige Verbindungen aus - erhitzter Glukose | and R. H. WALTER, I. S. FAGERSON. 1968. Journal of Food Science. 33(3): 294-297.
- Neue flüchtige Bestandteile von Röstkaffee | J. Stoffelsma, G. Sipma, D. K. Kettenes, and J. Pypker. 1968. J. Agric. Food Chem. 16, 6: 1000–1004.
- Bildung von fleischähnlichen Aromastoffen durch thermische Reaktion von Inosin-5'-monophosphat mit Cystein und Glutathion | Yuangang Zhang and Chi Tang Ho. 1991. J. Agric. Food Chem. 39, 6: 1145–1148.
- Eine katalytische, Me2Zn-vermittelte, enantioselektive Reformatsky-Reaktion mit Ketonen | and Pier Giorgio Cozzi Prof. Dr. 2006. Angewandte Chemie. 118(18): 3017-3020.
- Durch Indolinylmethanol katalysierte enantioselektive Reformatsky-Reaktion mit Ketonen | N Lin, MM Chen, RS Luo, YQ Deng, G Lu. 2010. Tetrahedron: Asymmetry. 21(23): 2816-2824.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
2-Furylacetone, 5 g | sc-265703 | 5 g | $132.00 |
