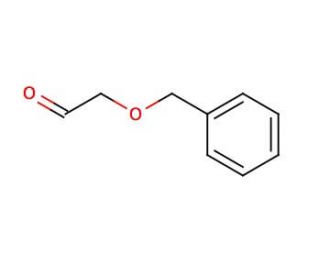
2-(Benzyloxy)acetaldehyde (CAS 60656-87-3)
Direktverknüpfungen
2-(Benzyloxy)acetaldehyd ist eine Verbindung, die aufgrund ihrer funktionellen Gruppen, die sie zu einem Zwischenprodukt in einer Vielzahl von Synthesewegen machen, in der organischen Chemieforschung verwendet wird. Sie wird häufig bei der Bildung heterocyclischer Verbindungen und als Aldehydkomponente in Aldol- und anderen Kohlenstoff-Kohlenstoff-Bindungsreaktionen eingesetzt. Der Benzyloxyrest dient als Schutzgruppe, die unter bestimmten Bedingungen entfernt werden kann, um selektive Umwandlungen zu ermöglichen. Studien mit 2-(Benzyloxy)acetaldehyd konzentrieren sich häufig auf die Optimierung der Reaktionsbedingungen, um die Ausbeute und Selektivität für die Zielmoleküle zu erhöhen. Darüber hinaus wird diese Verbindung zur Untersuchung von Mechanismen chemischer Reaktivität und zur Entwicklung neuer Synthesemethoden verwendet. Seine Stabilität unter verschiedenen Reaktionsbedingungen und die Fähigkeit, eine komplexe Molekülstruktur zu schaffen, sind Aspekte, die typischerweise untersucht werden, um den Nutzen von 2-(Benzyloxy)acetaldehyd in der synthetischen organischen Chemie zu erweitern.
2-(Benzyloxy)acetaldehyde (CAS 60656-87-3) Literaturhinweise
- Auf dem Weg zur Totalsynthese von Disorazol A(1) und C(1): asymmetrische Synthese eines maskierten Südsegments. | Hartung, IV., et al. 2002. Org Lett. 4: 3239-42. PMID: 12227758
- Synthese und Bewertung von optisch reinen Dioxolanen als Inhibitoren der RNA-Replikation des Hepatitis-C-Virus. | Bera, S., et al. 2003. Bioorg Med Chem Lett. 13: 4455-8. PMID: 14643345
- Eine intramolekulare 1,3-dipolare Cycloaddition zur Synthese von chiralen Azetidin-Nukleosid-Analoga: der D-Gluco-Fall. | Pádár, P., et al. 2005. Nucleosides Nucleotides Nucleic Acids. 24: 743-5. PMID: 16248028
- Einzelne Diastereomere von polyhydroxylierten 9-Oxa-1-azabicyclo[4.2.1]nonanen aus intramolekularer 1,3-dipolarer Cycloaddition von omega-ungesättigten Nitronen. | Padar, P., et al. 2006. J Org Chem. 71: 8669-72. PMID: 17064056
- Zusammenhang zwischen der Methylierung des VGF- und PGP9.5-Promotors und der Progression von Eierstockkrebs. | Brait, M., et al. 2013. PLoS One. 8: e70878. PMID: 24086249
- Eine Kurzsynthese von d-[1-(14) C]-Serin mit hoher enantiomerer Reinheit. | Song, F., et al. 2015. J Labelled Comp Radiopharm. 58: 173-6. PMID: 25728900
- Achmatowicz-Reaktion und ihre Anwendung bei der Synthese bioaktiver Moleküle. | Ghosh, AK. and Brindisi, M. 2016. RSC Adv. 6: 111564-111598. PMID: 28944049
- Eine Brønsted-Säure-katalysierte Kaskadenreaktion zur Umwandlung von Indolen in α-(3-Indolyl)-Ketone unter Verwendung von 2-Benzyloxy-Aldehyden. | Banerjee, A. and Maji, MS. 2019. Chemistry. 25: 11521-11527. PMID: 31283058
- Ausgewogenheit von Skelett und funktionellen Gruppen in Totalsynthesen komplexer Naturstoffe: eine Fallstudie über Tigliane, Daphnane und Ingenane Diterpenoide. | Liu, Z., et al. 2021. Nat Prod Rep. 38: 1589-1617. PMID: 33508045
- Untersuchung der Kompatibilität zwischen Sprengköpfen und peptidomimetischen Sequenzen von Proteaseinhibitoren - eine umfassende Reaktivitäts- und Selektivitätsstudie. | Müller, P., et al. 2023. Int J Mol Sci. 24: PMID: 37108388
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
2-(Benzyloxy)acetaldehyde, 1 g | sc-208936 | 1 g | $93.00 |
