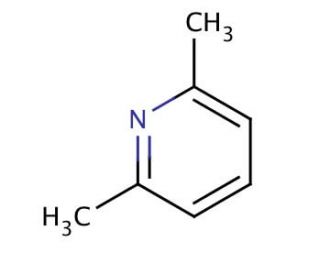
Molekülstruktur von 2,6-Lutidine, CAS-Nummer: 108-48-5
2,6-Lutidine (CAS 108-48-5)
CAS Nummer:
108-48-5
Molekulargewicht:
107.15
Summenformel:
C7H9N
Ergänzende Informationen:
Dieses Produkt wird als Gefahrgut eingestuft und unterliegt möglicherweise zusätzlichen Versandkosten.
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
2,6-Lutidin ist eine aromatische heterocyclische Verbindung, die in verschiedenen organischen Lösungsmitteln löslich ist. Diese Verbindung spielt eine Rolle als Zwischenprodukt bei der Herstellung verschiedener Farbstoffe und anderer chemischer Substanzen. Darüber hinaus hat es eine breite Anwendung bei der Synthese anderer aromatischer Verbindungen, einschließlich 2,6-Dihydropyridin und 2,6-Dimethoxypyridin.
2,6-Lutidine (CAS 108-48-5) Literaturhinweise
- Syntheseverfahren im Kilomaßstab für 2'-O-(2-Methoxyethyl)-Pyrimidin-Derivate. | Ross, BS., et al. 2005. Nucleosides Nucleotides Nucleic Acids. 24: 815-8. PMID: 16248042
- Eine Reihe von einkernigen quasi-zwei-koordinierten Kupfer(I)-Komplexen mit einem sterisch anspruchsvollen Thiolat-Liganden. | Groysman, S. and Holm, RH. 2009. Inorg Chem. 48: 621-7. PMID: 19138143
- Mizellen eines Diblock-Copolymers aus Styrol und Ethylenoxid in Mischungen aus 2,6-Lutidin und Wasser. | Tuzar, Z., et al. 2008. Langmuir. 24: 13863-5. PMID: 19360951
- Kupfer-katalysierte, aerobe oxidative Kreuzkupplung von Alkinen mit Arylboronsäuren: bemerkenswerte Selektivität in 2,6-Lutidin-Medien. | Yasukawa, T., et al. 2011. Org Biomol Chem. 9: 6208-10. PMID: 21808793
- Oxoammoniumsalz-Oxidationen von Alkoholen in Gegenwart von Pyridinbasen. | Bobbitt, JM., et al. 2014. J Org Chem. 79: 1055-67. PMID: 24386938
- Elektrophile Phosphoniumkation-vermittelte Phosphanoxid-Reduktion mit Oxalylchlorid und Wasserstoff. | Stepen, AJ., et al. 2018. Angew Chem Int Ed Engl. 57: 15253-15256. PMID: 30230149
- Chemie des Bis(pentalen)dititan: Aktivierung von C-H-, C-X- und H-H-Bindungen. | Tsoureas, N., et al. 2018. Dalton Trans. 47: 14531-14539. PMID: 30252008
- Zugang zu stereodefinierten (E)-2-Silylallylboronaten über regioselektive Chloroboration von Allenylsilanen. | Yang, Z., et al. 2019. Org Lett. 21: 9541-9544. PMID: 31713429
- Photochemische Umwandlung von Isoxazolen zu 5-Hydroxyimidazolinen. | Morita, T., et al. 2020. Org Lett. 22: 3460-3463. PMID: 32286839
- Mechanistische Details der metallfreien Cyclisierungsreaktion von Organophosphoroxid mit Alkinen unter Vermittlung von 2,6-Lutidin und Tf2 O. | Tian, J., et al. 2020. J Comput Chem. 41: 1709-1717. PMID: 32323872
- Eingeschlossene Wassermoleküle in binären Mischungen von Wasser und 2,6-Lutidin in der Nähe der unteren kritischen Lösungstemperatur. | Korotkevich, AA. and Bakker, HJ. 2021. J Phys Chem B. 125: 287-296. PMID: 33370126
- Calcium-vermittelte C(sp3)-H-Aktivierung und Alkylierung von Alkylpyridinen. | Zheng, X., et al. 2021. Inorg Chem. 60: 5114-5121. PMID: 33728911
- Photoredox-katalysierte intramolekulare Cyclopropanierung von Alkenen mit α-Brom-β-keto-Estern. | Ide, K., et al. 2021. Org Biomol Chem. 19: 9172-9176. PMID: 34664610
- Effiziente Reinigung von 2,6-Lutidin durch nicht-poröse adaptive Kristalle aus Pillararenen. | Wang, Z., et al. 2022. ACS Appl Mater Interfaces. 14: 41072-41078. PMID: 36053117
- Synthese von β,β-disubstituierten Styrolen über Trimethylsilyltrifluormethansulfonat-geförderte Aldehyd-Aldehyd-Aldol-Kopplungs-Elimination. | Dixon, GJ., et al. 2022. J Org Chem. 87: 14846-14854. PMID: 36239694
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
2,6-Lutidine, 25 ml | sc-238428 | 25 ml | $87.00 |
