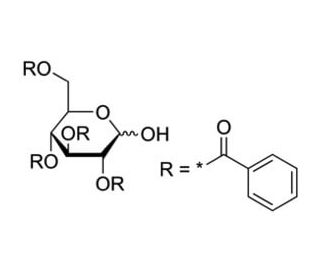
2,3,4,6-Tetra-O-benzoyl-D-glucopyranose (CAS 64768-20-3)
Direktverknüpfungen
2,3,4,6-Tetra-O-benzoyl-D-glucopyranose ist ein benzoylgeschütztes Glukosederivat, das in der Glykosylierungsforschung weit verbreitet ist. Die Benzoylgruppen schützen die Hydroxylfunktionen, was die Selektivität bei chemischen Reaktionen erhöht und die Synthese von Glykosyldonoren erleichtert. Diese Verbindung wird hauptsächlich als Zwischenprodukt in der Kohlenhydratchemie für die Synthese komplexer Oligosaccharide und Glykokonjugate verwendet. Durch die selektive Entfernung von Benzoylgruppen können Forscher andere funktionelle Gruppen an bestimmten Positionen einführen und so die Bildung von glykosidischen Bindungen genau kontrollieren. Diese Verbindung ermöglicht es Wissenschaftlern, die Stereochemie von Glykosylierungsreaktionen zu erforschen. Indem sie die Beteiligung benachbarter Gruppen kontrollieren, erreichen sie die gewünschte Stereoselektivität bei der Bildung glykosidischer Bindungen. Diese Eigenschaft ist entscheidend für die Herstellung von beta- oder alpha-verknüpften Sacchariden, die natürliche Glykane in Bezug auf Struktur und Funktion genau imitieren. In den Glykowissenschaften hilft 2,3,4,6-Tetra-O-benzoyl-D-glucopyranose bei der Synthese von Glycomimetika und Glykan-Arrays, die bei der Untersuchung von Kohlenhydrat-Protein-Wechselwirkungen verwendet werden. Auf diese Weise können Forscher glykanbindende Proteine identifizieren und ihre Spezifität bei der molekularen Erkennung untersuchen. Darüber hinaus hilft diese Verbindung bei der Untersuchung enzymatischer Prozesse wie Glykosyltransferase- oder Glykosidase-Reaktionen, indem sie als Substratmodell dient und Einblicke in die Enzymkinetik und Substratspezifität gewährt. Damit spielt sie eine wichtige Rolle bei der Weiterentwicklung der Glykosylierungsforschung und der Aufklärung der Funktion von Kohlenhydraten in verschiedenen biologischen Systemen.
2,3,4,6-Tetra-O-benzoyl-D-glucopyranose (CAS 64768-20-3) Literaturhinweise
- Eine neue, effiziente Glykosylierungsmethode für die Oligosaccharidsynthese unter neutralen Bedingungen: Herstellung und Verwendung neuer DISAL-Donatoren. | Petersen, L. and Jensen, KJ. 2001. J Org Chem. 66: 6268-75. PMID: 11559173
- Eine neue Glykosidierungsmethode durch Nitritverdrängung an substituierten Nitrobenzolen. | Alvarez-Micó, X., et al. 2007. Carbohydr Res. 342: 440-7. PMID: 17182018
- Überarbeitung des Konzepts 'bewaffnet-entwaffnet': die Bedeutung der anomeren Konfiguration bei der Aktivierung von S-Benzoxazolylglykosiden. | Crich, D. and Li, M. 2007. Org Lett. 9: 4115-8. PMID: 17887763
- Stereoselektive direkte Glykosylierung mit anomeren Hydroxyzuckern durch Aktivierung mit Phthalsäureanhydrid und Trifluormethansulfonsäureanhydrid unter Einbeziehung von Glykosylphthalat-Zwischenprodukten. | Kim, KS., et al. 2008. J Am Chem Soc. 130: 8537-47. PMID: 18528988
- OFox-Imidate als vielseitige Glykosylspender für die chemische Glykosylierung. | Nigudkar, SS., et al. 2017. Org Biomol Chem. 15: 348-359. PMID: 27808325
- Ein adressierbarer 2D-heterogener Nanoreaktor zur Untersuchung der enzymkatalysierten Reaktion an der Grenzfläche. | Wang, D., et al. 2017. Small. 13: PMID: 28639303
- Hocheffiziente Glykosidierung von Glykosylchloriden durch kooperative Silber(I)-Oxid-Trifl-Säure-Katalyse. | Geringer, SA., et al. 2020. Chemistry. 26: 8053-8063. PMID: 32145116
- Direkte Glykosylierungen mit 1-Hydroxy-Glykosyl-Donatoren unter Verwendung von Trifluormethansulfonsäureanhydrid und Diphenylsulfoxid | Garcia, B. A., Poole, J. L., & Gin, D. Y. 1997. Journal of the American Chemical Society. 119(32): 7597-7598.
- Die Reaktion von Penta-O-Benzoyl-d-glucopyranose mit Piperidin: Charakterisierung der isolierten Produkte und Untersuchung des Reaktionsmechanismus | Salinas, A. E. 1999. Carbohydrate research. 316(1-4): 34-46.
- Chemoenzymatische Synthese von enantiomerenangereicherten Aminoalkenolen und deren Glykosiden | Ziegler, T., & Jurisch, C. 2000. Tetrahedron: Asymmetry. 11(16): 3403-3418.
- NaBH3CN und andere Systeme als Ersatz für Zinn- und Siliziumhydride bei der licht- oder wärmeinitiierten Reduktion von Halogenzuckern: ein abstimmbarer Zugang zu 2-Desoxyzuckern oder 1,5-Anhydroitolen | Bruyere, I., Toth, Z., Benyahia, H., Xue, J. L., & Praly, J. P. 2013. Tetrahedron. 69(46): 9656-9662.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
2,3,4,6-Tetra-O-benzoyl-D-glucopyranose, 250 mg | sc-288397 | 250 mg | $209.00 | |||
2,3,4,6-Tetra-O-benzoyl-D-glucopyranose, 1 g | sc-288397A | 1 g | $559.00 |
