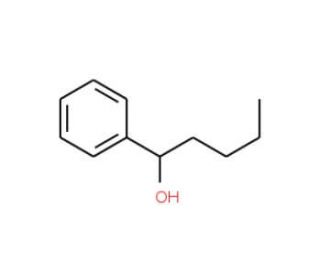
Molekülstruktur von 1-Phenyl-1-pentanol, CAS-Nummer: 583-03-9
1-Phenyl-1-pentanol (CAS 583-03-9)
Alternative Namen:
n-Butyl phenyl carbinol
CAS Nummer:
583-03-9
Molekulargewicht:
164.24
Summenformel:
C11H16O
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
1-Phenyl-1-pentanol ist ein chemisches Zwischenprodukt in der organischen Synthese. Es wirkt als Nukleophil in verschiedenen Reaktionen und ist an Prozessen wie Grignard-Reaktionen und nukleophiler Substitution beteiligt. 1-Phenyl-1-Pentanol kann auch als chirales Hilfsmittel dienen und die asymmetrische Synthese organischer Moleküle erleichtern. Auf molekularer Ebene interagiert 1-Phenyl-1-Pentanol mit anderen Reagenzien, um neue Kohlenstoff-Kohlenstoff- oder Kohlenstoff-Heteroatom-Bindungen zu bilden, und trägt so zum Aufbau komplexer Molekularstrukturen bei. Sein Wirkmechanismus umfasst die Bildung von Zwischenprodukten, die durch weitere Umwandlungen zu den gewünschten Produkten führen.
1-Phenyl-1-pentanol (CAS 583-03-9) Literaturhinweise
- Stereoselektive 1,2-Additionen von alpha-Alkoxymethyllithium an Aldehyde. | Smyj, RP. and Chong, JM. 2001. Org Lett. 3: 2903-6. PMID: 11529786
- Regioselektive Einführung von Elektrophilen in die 4-Position von 1-Hydroxypyrazol über Brom-Lithium-Austausch. | Balle, T., et al. 1999. J Org Chem. 64: 5366-5370. PMID: 11674594
- Ein hoch enantioselektiver Phosphabicyclooctan-Katalysator für die kinetische Trennung von Benzylalkoholen. | Vedejs, E. and Daugulis, O. 2003. J Am Chem Soc. 125: 4166-73. PMID: 12670239
- Confronto tra Chirasil-DEX CB come fase stazionaria gascromatografica e ULMO come fase stazionaria cromatografica liquida per l'enantioseparazione di aril- ed eteroarilcarbinoli. | Uray, G., et al. 2003. J Chromatogr A. 992: 151-7. PMID: 12735471
- Oxidative kinetische Trennung racemischer Alkohole, katalysiert durch chirale Ferrocenyloxazolinylphosphin-Ruthenium-Komplexe. | Nishibayashi, Y., et al. 2003. J Org Chem. 68: 5875-80. PMID: 12868920
- Konkurrierende Reaktionen von sekundären Alkoholen mit Natriumhypochlorit, gefördert durch Phasentransferkatalyse. | Bright, ZR., et al. 2005. J Org Chem. 70: 684-7. PMID: 15651819
- Nickel-katalysierte Alkylierung von Aldehyden mit Trialkylboranen. | Hirano, K., et al. 2005. Org Lett. 7: 4689-91. PMID: 16209511
- Kinetische Trennung racemischer sekundärer Alkohole, katalysiert durch chirale Diaminodiphosphin-Ir(I)-Komplexe. | Li, YY., et al. 2006. Org Lett. 8: 5565-7. PMID: 17107073
- Fortschritte bei der asymmetrischen oxidativen kinetischen Auflösung von racemischen sekundären Alkoholen, katalysiert durch chirale Mn(III)-Salenkomplexe. | Ahmad, I., et al. 2017. Chirality. 29: 798-810. PMID: 28963733
- [Experimentelle Untersuchung der choleretischen Aktivität von 2'Hydroxy-5'carboxy-1-phenyl-1-pentanol]. | Van den Driessche, J., et al. 1968. Therapie. 23: 329-40. PMID: 5701508
- Studien über die Wechselwirkungen von chiralen sekundären Alkoholen mit der Hydroxysteroid-Sulfotransferase STa der Ratte. | Banoglu, E. and Duffel, MW. 1997. Drug Metab Dispos. 25: 1304-10. PMID: 9351908
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
1-Phenyl-1-pentanol, 10 g | sc-273438 | 10 g | $54.00 |
