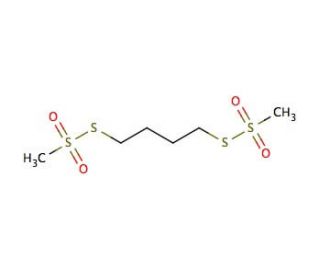
1,4-Butanediyl Bismethanethiosulfonate (CAS 55-99-2)
Produktreferenzen ansehen (2)
Direktverknüpfungen
1,4-Butandiylbismethanthiosulfonat ist eine chemische Verbindung, die in der Protein- und Peptidforschung als spaltbarer Vernetzer eingesetzt wird. Forscher nutzen diese Verbindung wegen ihrer Fähigkeit, reversible Disulfidbindungen zwischen Thiolgruppen von Cysteinresten zu bilden, was bei der Untersuchung von Proteinstrukturen und -interaktionen nützlich sein kann. In der Proteomik wird 1,4-Butandiylbismethanthiosulfonat zur Stabilisierung von Proteinkomplexen für die massenspektrometrische Analyse eingesetzt, was ein genaueres Verständnis der Protein-Protein-Wechselwirkungen ermöglicht. Es ist auch an der reversiblen Modifizierung von Cysteinresten in Enzymen und anderen Proteinen beteiligt, was zur Aufklärung ihrer Funktionen und Mechanismen beiträgt. Darüber hinaus spielt diese Verbindung eine Rolle im Bereich der Materialwissenschaften, wo sie zur Modifizierung der Oberfläche von Goldnanopartikeln verwendet wird, indem sie eine reversible Verbindung für die Anbringung thiolhaltiger Moleküle bereitstellt.
1,4-Butanediyl Bismethanethiosulfonate (CAS 55-99-2) Literaturhinweise
- Nachweis von sowohl extra- als auch intrazellulären Cysteinzielen für die Proteinmodifikation zur Aktivierung der RET-Kinase. | Akhand, AA., et al. 2002. Biochem Biophys Res Commun. 292: 826-31. PMID: 11944888
- Redox-Kontrolle der katalytischen Aktivitäten von membranassoziierten Proteintyrosinkinasen. | Nakashima, I., et al. 2005. Arch Biochem Biophys. 434: 3-10. PMID: 15629102
- Ein Vergleich der elektrophysiologischen Eigenschaften der CNGA1-, CNGA1tandem- und CNGA1cys-freien Kanäle. | Mazzolini, M., et al. 2008. Eur Biophys J. 37: 947-59. PMID: 18379773
- Bewegungen des nativen C505 während des Kanalgatings in CNGA1-Kanälen. | Nair, AV., et al. 2009. Eur Biophys J. 38: 465-78. PMID: 19132361
- Konformationsumlagerungen in der S6-Domäne und dem C-Linker während des Gating in CNGA1-Kanälen. | Nair, AV., et al. 2009. Eur Biophys J. 38: 993-1002. PMID: 19488745
- 1,4-Butandiyl-Bismethanethiosulfonat (BMTS) induziert Apoptose durch einen von reaktiven Sauerstoffspezies vermittelten Mechanismus. | Hossain, K., et al. 2009. J Cell Biochem. 108: 1059-65. PMID: 19830705
- Strukturanalyse des extrazellulären Eingangs zum Permeationsweg des Serotonintransporters. | Torres-Altoro, MI., et al. 2010. J Biol Chem. 285: 15369-15379. PMID: 20304925
- Kontrolle von genetisch vorgegebenen Protein-Tyrosinkinase-Aktivitäten durch umweltbedingte Redoxreaktionen. | Nakashima, I., et al. 2011. Enzyme Res. 2011: 896567. PMID: 21755044
- Die ATPase-Aktivität der P-Glykoprotein-Arzneimittelpumpe wird stark aktiviert, wenn die N-terminalen und zentralen Regionen der Nukleotid-Bindungsdomänen eng miteinander verbunden sind. | Loo, TW., et al. 2012. J Biol Chem. 287: 26806-16. PMID: 22700974
- Identifizierung des Abstands zwischen den homologen Hälften des P-Glykoproteins, der den Wechsel zwischen hoher und niedriger ATPase-Aktivität auslöst. | Loo, TW. and Clarke, DM. 2014. J Biol Chem. 289: 8484-92. PMID: 24523403
- Die Einschränkung der lateralen Helix des Atmungskomplexes I durch Quervernetzung beeinträchtigt weder die Enzymaktivität noch die Protonenverschiebung. | Zhu, S. and Vik, SB. 2015. J Biol Chem. 290: 20761-20773. PMID: 26134569
- Ein kurzer Vernetzer aktiviert das menschliche P-Glykoprotein, dem ein katalytisches Carboxylat fehlt. | Loo, TW. and Clarke, DM. 2017. Biochem Pharmacol. 145: 27-33. PMID: 28837794
- Aktivierungs- und Inaktivierungsmechanismen der menschlichen spannungsgesteuerten KV4-Kanalkomplexe im geschlossenen Zustand. | Ye, W., et al. 2022. Mol Cell. 82: 2427-2442.e4. PMID: 35597238
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
1,4-Butanediyl Bismethanethiosulfonate, 25 mg | sc-208789 | 25 mg | $330.00 |
