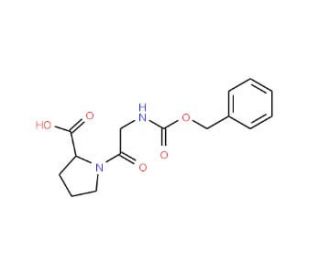
Z-Gly-Pro-OH (CAS 1160-54-9)
LINKS RÁPIDOS
O Z-Gly-Pro-OH é um dipeptídeo cíclico, constituído por dois aminoácidos ligados por uma ligação peptídica. Desempenha um papel vital em numerosos processos, atraindo uma atenção significativa na investigação científica. As aplicações de investigação científica do Z-Gly-Pro-OH têm sido diversas e impactantes. Os investigadores utilizaram-na extensivamente para aprofundar as estruturas e funções de proteínas, péptidos e enzimas. Além disso, tem sido um recurso valioso no estudo das membranas celulares e das vias de sinalização, revelando conhecimentos fundamentais sobre os processos celulares. Além disso, a contribuição da Z-Gly-Pro-OH para a compreensão do ADN, do ARN e das vias metabólicas não pode ser negligenciada. Quanto ao seu mecanismo de ação, subsistem algumas incertezas. No entanto, postula-se que o dipeptídeo cíclico se liga a proteínas e peptídeos específicos, desencadeando assim uma cascata de interacções que regulam processos celulares vitais. Por exemplo, observou-se que se liga a certas enzimas, facilitando a catálise da formação de novas moléculas ou a quebra de moléculas existentes.
Z-Gly-Pro-OH (CAS 1160-54-9) Referencias
- O domínio beta-propulsor não catalítico da prolil oligopeptidase aumenta a capacidade catalítica do domínio da peptidase. | Szeltner, Z., et al. 2000. J Biol Chem. 275: 15000-5. PMID: 10747969
- Competência dependente do substrato da tríade catalítica da prolil oligopeptidase. | Szeltner, Z., et al. 2002. J Biol Chem. 277: 44597-605. PMID: 12228249
- Caracterização do sítio ativo de uma endopeptidase de clivagem pós-prolina recém-descoberta e potencialmente significativa, denominada ZIP, utilizando LC-UV-MS. | McMahon, G., et al. 2003. Analyst. 128: 670-5. PMID: 12866886
- Análogos do tripeptídeo neuroprotector Gly-Pro-Glu (GPE): síntese e relações estrutura-atividade. | Alonso De Diego, SA., et al. 2005. Bioorg Med Chem Lett. 15: 2279-83. PMID: 15837309
- Propriedades do homólogo da prolil oligopeptidase de Pyrococcus furiosus. | Juhász, T., et al. 2006. FEBS Lett. 580: 3493-7. PMID: 16714022
- Alterações conformacionais induzidas por ligandos na prolil oligopeptidase: uma abordagem cinética. | Van Elzen, R., et al. 2017. Protein Eng Des Sel. 30: 217-224. PMID: 28062644
- Cianação descarboxilativa de ácidos carboxílicos à temperatura ambiente utilizando catálise fotoredox e cianobenziodoxolonas: um mecanismo divergente em comparação com a alquinilação. | Le Vaillant, F., et al. 2017. Chem Sci. 8: 1790-1800. PMID: 28451301
- Colagenase de Clostridium histolyticum: desenvolvimento de novos substratos de tioésteres, fluorogénicos e depsipeptídeos e de novos inibidores. | Vencill, CF., et al. 1985. Biochemistry. 24: 3149-57. PMID: 2992578
- Ciclobutilação fotoquímica de radicais centrados em C(sp3)-C. | Ernouf, G., et al. 2020. Angew Chem Int Ed Engl. 59: 2618-2622. PMID: 31599038
- Estudos dos requisitos de substrato, propriedades cinéticas e inibidores competitivos das enzimas que catabolizam a TRH no cérebro do rato. | Busby, WH., et al. 1982. Brain Res. 242: 261-70. PMID: 6126250
- Estudos de RMN de um tetrapeptídeo livre e protegido, a glicil-L-prolilglicilglicina, em meio de suporte beta-torno. | Perly, B., et al. 1983. Biopolymers. 22: 1853-68. PMID: 6616010
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Z-Gly-Pro-OH, 1 g | sc-296758 | 1 g | $70.00 | |||
Z-Gly-Pro-OH, 5 g | sc-296758A | 5 g | $206.00 |
