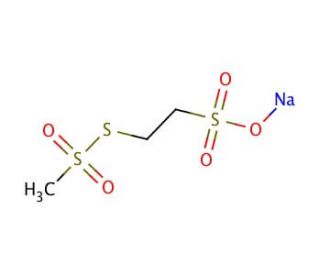
Sodium (2-Sulfonatoethyl)methanethiosulfonate (CAS 184644-83-5)
Veja citações de produtos (1)
LINKS RÁPIDOS
O (2-sulfonatoetil)metanotiossulfonato de sódio é uma sonda para os canais dos receptores GABAA. Como metanotiossulfonato, o (2-sulfonatoetil)metanotiossulfonato de sódio é reativo à sulfidrila e pode ser utilizado para estudar os resíduos de cisteína nas proteínas. O (2-sulfonatoetil)metanotiossulfonato de sódio reage específica e rapidamente com tióis para formar dissulfuretos mistos. O (2-sulfonatoetil)metanotiossulfonato de sódio sonda as estruturas do canal do recetor ACh, do canal do recetor GABAA e da permease da lactose. O (2-sulfonatoetil)metanotiossulfonato de sódio é particularmente eficaz na sondagem de proteínas nativas associadas a membranas, tais como canais e transportadores.
Sodium (2-Sulfonatoethyl)methanethiosulfonate (CAS 184644-83-5) Referencias
1. Dunten, R.L., et al.: Biochem., 32, 3139 (1993),2. Yang, N. et al.: Neuron, 16, 113 (1996),
3. Holmgren, M., et al: Neuropharmacology, 35, 797 (1996),
4. Chahine, M., et al.: Biochem. Bio. Res. Commun., 233, 606 (1997),
5. Ehrlich, B.E., et al.: J. Gen. Physiol., 109, 255 (1997),
6. Lang, R.J., Harvey, J.R., and Mulholland, E.L.Sodium (2-sulfonatoethyl) methanethiosulfonate prevents S-nitroso-L-cysteine activation of Ca2+-activated K+ (BKCa) channels in myocytes of the guinea-pig taenia caeca. Br. J. Pharmacol. 139(6), 1153-1163 (2003).
7. Li, R.A., Tsushima, R.G., Kallen, R.G., et al.Pore residues critical for μ-CTX binding to rat skeletal muscle Na+ channels revealed by cysteine mutagenesis. Biophys. J. 73(4), 1874-1884 (1997).
8. Guan, L., and Kaback, H.R.Site-directed alkylation of cysteine to test solvent accessibility of membrane proteins. Nature Protocols 2(8), 2012-2017 (2007).
9. Engh, A.M., and Maduke, M.Cysteine accessibility in ClC-0 supports conservation of the ClC intracellular vestibule. Journal of General Physiology 125(6), 601-617 (2014).
10. Liu, X., Alexander, C., Serrano, J., et al.Variable reactivity of an engineered cysteine at position 338 in cystic fibrosis transmembrane conductance regulator reflects different chemical states of the thiol. The Journal of Biological Chemisty 281(12), 8275-8285 (2006).
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Sodium (2-Sulfonatoethyl)methanethiosulfonate, 250 mg | sc-212933 | 250 mg | $370.00 |
