Subscrever / Inscrever-se Conta
Corrinho de compra (0)
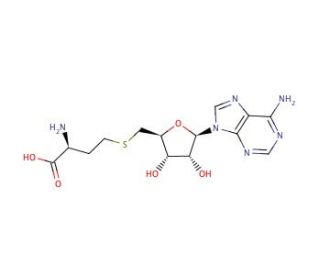
Estrutura molecular do S-(5'-Adenosyl)-L-homocysteine, Número CAS: 979-92-0
S-(5′-Adenosyl)-L-homocysteine (CAS 979-92-0)
Nomes alternativos:
5′-Deoxy-S-adenosyl-L-homocysteine; AdoHcy; S-(5′-Deoxyadenosine-5′)-L-homocysteine
Aplicacao:
S-(5'-Adenosyl)-L-homocysteine é um derivado de aminoácido que é um intermediário importante nas vias metabólicas
Numero VAT:
979-92-0
Privada:
≥98%
Peso Molecular:
384.41
Separar por Funcao:
C14H20N6O5S
Para uso em exclusivo em pesquisa. Não se destina a uso em diagnostico e tratamento.
* Refere-se a Certificado de Análise para data especifica de lotes (incluindo-se o conteúdo de agua).
LINKS RÁPIDOS
Informacoes sobre ordens
Descricao
Informações Técnicas
Informações de Segurança
SDS & Certificado de Análise
A S-(5'-Adenosil)-L-homocisteína é um derivado de aminoácido que é um intermediário importante nas vias metabólicas. As duas mais notáveis são o ciclo do metil ativado e a biossíntese da cisteína. Também é um produto da metilação de moléculas biológicas dependente de S-adenosil-metionina (SAM). É um intermediário importante no metabolismo da metionina, cisteína e outros compostos contendo enxofre.
S-(5′-Adenosyl)-L-homocysteine (CAS 979-92-0) Referencias
- Inibidores selectivos de proteínas metiltransferases. | Kaniskan, HÜ., et al. 2015. J Med Chem. 58: 1596-629. PMID: 25406853
- Cromatografia líquida de fase invertida e de permuta catiónica com deteção espectrofotométrica e elementar/espectrométrica de massa molecular para a relação S-adenosil metionina/S-adenosil homocisteína como índice de metilação em culturas celulares de cancro do ovário. | Iglesias González, T., et al. 2015. J Chromatogr A. 1393: 89-95. PMID: 25836049
- A Trimetilação de H3K9 Silencia a Expressão de Fas para Conferir ao Carcinoma do Cólon uma Fuga Imune e Quimioresistência ao 5-Fluorouracil. | Paschall, AV., et al. 2015. J Immunol. 195: 1868-82. PMID: 26136424
- LDOC1 silenciado pela exposição ao cigarro e envolvido na transformação neoplásica oral. | Lee, CH., et al. 2015. Oncotarget. 6: 25188-201. PMID: 26317789
- Um inibidor potente, seletivo e ativo nas células da proteína humana tipo I arginina metiltransferase. | Eram, MS., et al. 2016. ACS Chem Biol. 11: 772-781. PMID: 26598975
- Estudos da relação estrutura-atividade para inibidores do Enhancer of Zeste Homologue 2 (EZH2) e do Enhancer of Zeste Homologue 1 (EZH1). | Yang, X., et al. 2016. J Med Chem. 59: 7617-33. PMID: 27468126
- Descoberta de inibidores de bisubstrato da nicotinamida N-metiltransferase (NNMT). | Babault, N., et al. 2018. J Med Chem. 61: 1541-1551. PMID: 29320176
- Identificação de alcalóides de protoberberina como novos inibidores da histona metiltransferase G9a através de rastreio virtual baseado na estrutura. | Chen, J., et al. 2018. J Comput Aided Mol Des. 32: 917-928. PMID: 30171419
- Análogos do estado de transição da 5'-Metiltioadenosina nucleosidase de Campylobacter jejuni. | Ducati, RG., et al. 2018. ACS Chem Biol. 13: 3173-3183. PMID: 30339406
- Descoberta de um inibidor covalente de primeira classe da proteína arginina metiltransferase 6 (PRMT6). | Shen, Y., et al. 2020. J Med Chem. 63: 5477-5487. PMID: 32367723
- Descoberta baseada na estrutura de inibidores peptidomiméticos potentes para a proteína N-Terminal Metiltransferase 1. | Chen, D., et al. 2021. ACS Med Chem Lett. 12: 485-493. PMID: 33738076
- A metabolómica de alta cobertura revela a paisagem bioquímica do transporte inter-orgânico e da comunicação intestino-cérebro em ratos, impulsionada pelo microbiota. | Lai, Y., et al. 2021. Nat Commun. 12: 6000. PMID: 34667167
- Inibição potente da SARS-CoV-2 nsp14 N7-Methyltransferase por análogos de bisubstratos à base de sulfonamida. | Ahmed-Belkacem, R., et al. 2022. J Med Chem. 65: 6231-6249. PMID: 35439007
- Vigilância ecológica multiómica de contaminações complexas com um invertebrado estuarino adaptado localmente. | Hillyer, KE., et al. 2023. Environ Pollut. 319: 120993. PMID: 36623788
- Resposta pós-prandial no hepatopâncreas e na hemolinfa de Penaeus monodon alimentado com diferentes dietas. Informações ómicas sobre o metabolismo dos glicoconjugados, a utilização da energia, a biossíntese da quitina, a função imunitária e a autofagia. | Mendoza-Porras, O., et al. 2023. Comp Biochem Physiol Part D Genomics Proteomics. 46: 101073. PMID: 37018937
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
S-(5′-Adenosyl)-L-homocysteine, 5 mg | sc-215826B | 5 mg | $46.00 | |||
S-(5′-Adenosyl)-L-homocysteine, 10 mg | sc-215826 | 10 mg | $82.00 | |||
S-(5′-Adenosyl)-L-homocysteine, 25 mg | sc-215826A | 25 mg | $122.00 | |||
S-(5′-Adenosyl)-L-homocysteine, 50 mg | sc-215826C | 50 mg | $215.00 |
