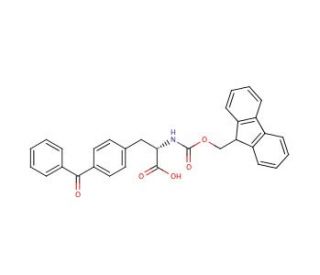
Fmoc-Bpa-OH (CAS 117666-96-3)
LINKS RÁPIDOS
O Fmoc-Bpa-OH é um composto que funciona como um bloco de construção versátil na síntese de péptidos. Actua como um grupo protetor para o grupo amino dos aminoácidos, permitindo uma desproteção selectiva e subsequentes reacções de acoplamento. O mecanismo de ação do Fmoc-Bpa-OH envolve a formação de ligações amida estáveis com aminoácidos, permitindo a montagem gradual de péptidos com elevada pureza e rendimento. O Fmoc-Bpa-OH facilita a síntese de péptidos complexos, fornecendo um meio de controlar a reatividade de grupos funcionais específicos, conduzindo à construção precisa de cadeias peptídicas. O seu papel na síntese de péptidos envolve a proteção de grupos amino, evitando reacções laterais indesejadas e assegurando a formação bem sucedida de ligações peptídicas. O mecanismo de ação do Fmoc-Bpa-OH a nível molecular permite a síntese eficiente e controlada de péptidos com sequências e estruturas adaptadas, tornando-o uma ferramenta útil na investigação e desenvolvimento da química dos péptidos.
Fmoc-Bpa-OH (CAS 117666-96-3) Referencias
- Papel duplo da BAD pró-apoptótica na secreção de insulina e na sobrevivência das células beta. | Danial, NN., et al. 2008. Nat Med. 14: 144-53. PMID: 18223655
- Síntese e caraterização espectroscópica de ligandos peptídicos de fotoafinidade para o estudo da interação da proteína rodopsina-G. | Chen, Y., et al. 2008. Photochem Photobiol. 84: 831-8. PMID: 18282180
- A histerese do gating sublinha a sensibilização dos canais TRPV3. | Liu, B., et al. 2011. J Gen Physiol. 138: 509-20. PMID: 22006988
- Manipulação da ativação do subtipo de recetor Y de análogos curtos do neuropeptídeo Y através da introdução de carbaboranos. | Hofmann, S., et al. 2013. Neuropeptides. 47: 59-66. PMID: 23352609
- Ativação direta da BAK pró-apoptótica de comprimento total. | Leshchiner, ES., et al. 2013. Proc Natl Acad Sci U S A. 110: E986-95. PMID: 23404709
- Síntese química de péptidos com hidrocarbonetos para a investigação da interação entre proteínas e para a orientação terapêutica. | Bird, GH., et al. 2011. Curr Protoc Chem Biol. 3: 99-117. PMID: 23801563
- A ligação do inibidor PA1b às subunidades c e e da ATPase vacuolar revela o seu mecanismo inseticida. | Muench, SP., et al. 2014. J Biol Chem. 289: 16399-408. PMID: 24795045
- A foto-lisina capta proteínas que ligam modificações pós-tradução da lisina. | Yang, T., et al. 2016. Nat Chem Biol. 12: 70-2. PMID: 26689789
- Abordagens de proteómica química e de 'Middle-Down' para revelar a dinâmica da modificação da histona H4 no ciclo celular: Semi-quantificação sem rótulo de modificações do péptido da cauda da histona, incluindo fosforilação e captura altamente sensível de proteínas de ligação a PTM de histonas utilizando reticuladores foto-reactivos. | Yamamoto, K., et al. 2015. Mass Spectrom (Tokyo). 4: A0039. PMID: 26819910
- Péptidos curtos dirigidos à integrase do VIH-1 derivados de uma sequência da proteína R viral. | Zhao, XZ., et al. 2018. Molecules. 23: PMID: 30049955
- Expressão livre de células e foto-reticulação do recetor humano do neuropeptídeo Y2. | Kögler, LM., et al. 2019. Front Pharmacol. 10: 176. PMID: 30881304
- Seleção bacteriana e libertação desencadeada pela infeção de conjugados antibióticos de colistina. | Tegge, W., et al. 2021. Angew Chem Int Ed Engl. 60: 17989-17997. PMID: 34097810
- A dinâmica conformacional ligada ao fecho do domínio e à ligação do substrato explica o mecanismo de regulação alostérica do ERAP1. | Maben, Z., et al. 2021. Nat Commun. 12: 5302. PMID: 34489420
- Identificação do local de interação entre a semaforina-3A e o seu péptido inibitório. | Kretschmer, K., et al. 2023. J Pept Sci. 29: e3460. PMID: 36285908
- A vacinação profiláctica e terapêutica protege a saúde do esperma contra as anomalias induzidas pela Chlamydia muridarum. | Bryan, ER., et al. 2023. Biol Reprod. 108: 758-777. PMID: 36799886
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Fmoc-Bpa-OH, 1 g | sc-223992 | 1 g | $309.00 |
