Subscrever / Inscrever-se Conta
Corrinho de compra (0)
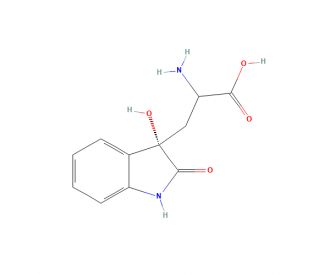
Estrutura molecular do Dioxindolyl-L-alanine, Número CAS: 184955-21-3
Dioxindolyl-L-alanine (CAS 184955-21-3)
Nomes alternativos:
(αS)-α-Amino-2,3-dihydro-3-hydroxy-2-oxo-1H-indole-3-propanoic Acid
Numero VAT:
184955-21-3
Peso Molecular:
236.22
Separar por Funcao:
C11H12N2O4
Para uso em exclusivo em pesquisa. Não se destina a uso em diagnostico e tratamento.
* Refere-se a Certificado de Análise para data especifica de lotes (incluindo-se o conteúdo de agua).
LINKS RÁPIDOS
Informacoes sobre ordens
Descricao
Informações Técnicas
Informações de Segurança
SDS & Certificado de Análise
A dioxindolil-L-alanina desempenha um papel no campo da síntese de péptidos, particularmente na criação de péptidos enriquecidos com aminoácidos únicos, como o 5-hidroxitriptofano, a oxindolilalanina, a N-formilquinurenina e a quinurenina. A sua utilidade decorre da sua capacidade de introduzir estes aminoácidos especializados em cadeias peptídicas, permitindo assim aos investigadores explorar as vias e mecanismos bioquímicos em que estes aminoácidos participam. Especificamente, a inclusão de Dioxindolil-L-alanina na síntese de péptidos facilita o estudo do metabolismo do triptofano e dos seus efeitos a jusante, que são fundamentais para a compreensão de vários processos e respostas biológicas.
Dioxindolyl-L-alanine (CAS 184955-21-3) Referencias
- O indole pode atuar como um sinal extracelular para regular a formação de biofilme de Escherichia coli e de outras bactérias produtoras de indole. | Martino, PD., et al. 2003. Can J Microbiol. 49: 443-9. PMID: 14569285
- Mecanismo de ligação de análogos de substratos à triptofano indol-liase: estudos utilizando espetrofotometria de varrimento rápido e de fluxo interrompido de comprimento de onda único. | Phillips, RS., et al. 1990. Biochemistry. 29: 8608-14. PMID: 2271544
- Uma prova cinética direta da coexistência de 'adaptação induzida' e 'adaptação selecionada' no mecanismo de reação de uma triptofano indol liase Y72F mutante de Proteus vulgaris. | Faleev, NG., et al. 2014. Biochim Biophys Acta. 1844: 1860-7. PMID: 25084024
- A estrutura cristalina de Proteus vulgaris triptofano indol-liase complexada com oxindolil-L-alanina: implicações para o mecanismo de reação. | Phillips, RS., et al. 2018. Acta Crystallogr D Struct Biol. 74: 748-759. PMID: 30082510
- Deteção e identificação de intermediários transitórios nas reacções da triptofano sintase com oxindolil-L-alanina e 2,3-di-hidro-L-triptofano. Evidência de um intermediário tetraédrico (gem-diamina). | Roy, M., et al. 1988. Biochemistry. 27: 8661-9. PMID: 3064816
- Bases Estruturais da Estereoquímica da Inibição da Triptofano Sintase pelo Triptofano e Derivados. | Phillips, RS. and Harris, AP. 2021. Biochemistry. 60: 231-244. PMID: 33428374
- Inibição diferencial da triptofano sintase e da triptofanase pelos dois diastereoisómeros do 2,3-dihidro-L-triptofano. Implicações para a estereoquímica dos intermediários da reação. | Phillips, RS., et al. 1985. J Biol Chem. 260: 14665-70. PMID: 3902836
- Interações da triptofano sintase, da triptofanase e do fosfato de piridoxal com a oxindolil-L-alanina e o 2,3-di-hidro-L-triptofano: apoio a um intermediário indoleno no metabolismo do triptofano. | Phillips, RS., et al. 1984. Biochemistry. 23: 6228-34. PMID: 6395894
- Triptofanase de Escherichia coli: propriedades catalíticas e espectrais em solventes orgânicos e água. | Faleev, NG., et al. 1994. Biochem Mol Biol Int. 34: 209-16. PMID: 7849621
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Dioxindolyl-L-alanine, 50 mg | sc-497015 | 50 mg | $434.00 |
