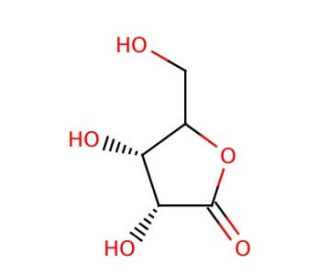
D-Ribonolactone 的分子结构, CAS编号: 5336-08-3
D-Ribonolactone (CAS 5336-08-3)
备用名:
D-(+)-Ribonic Acid γ-Lactone; D-(+)-Ribonolactone; D-Ribono-1,4-lactone
应用:
D-Ribonolactone 是一种糖内酯和∫-半乳糖苷酶抑制剂
CAS号码:
5336-08-3
纯度:
≥97%
分子量:
148.11
分子式:
C5H8O5
仅供科研使用。不可用于诊断或治疗。
* 参考分析证明 大量特定数据 (包括水 含量).
快捷链接
订购信息
描述
技术信息
安全信息
安全技术说明书和分析证明书
D-Ribonolactone 是一种从核糖中提取的环糖内酯,在各种研究工作中,尤其是在生物化学、酶学和有机合成领域,它已成为一种重要的分子。它的化学结构以五元内酯环为特征,有利于研究碳水化合物化学和酶转化。在研究中,D-核糖内酯可作为内酯酶和内酯化酶等酶的底物,催化其水解生成 D-核糖,D-核糖是一种参与多种生物过程的基本糖分子。人们对这种酶水解机制进行了广泛研究,以了解酶与底物之间的相互作用、催化机制和底物特异性,从而为酶动力学和蛋白质工程策略提供启示。此外,D-核糖内酯被用作合成含核糖化合物(包括核苷、核苷酸和碳水化合物衍生物)的前体,促进了新型生物大分子的开发,有望应用于药物发现、分子生物学和化学生物学研究。作为有机合成的起始原料,D-核苷酸的用途十分广泛,可以构建多种化学库和分子探针,用于研究生物系统和开发药物。总之,D-核糖酸内酯仍然是科学研究的重要工具,有助于推动碳水化合物化学、酶学和合成生物学的发展。
D-Ribonolactone (CAS 5336-08-3) 参考文献
- 在小鼠体内发现具有抗糖尿病活性的小分子胰岛素模拟物。 | Zhang, B., et al. 1999. Science. 284: 974-7. PMID: 10320380
- 从阿拉伯糖醇简易合成对映纯 C2 对称 1,2:4,5 二环氧戊烷和 '伪'-C2 对称 3-叠氮-1,2:4,5-二环氧戊烷。 | Boydell, AJ., et al. 2003. J Org Chem. 68: 8252-5. PMID: 14535812
- 利用分析保护剂补偿茶叶基质中 186 种农药的气相色谱-质谱分析中的基质效应。 | Li, Y., et al. 2012. J Chromatogr A. 1266: 131-42. PMID: 23102633
- 核苷CXLVIII.6-(beta-D-呋喃核糖基)吡啶酰胺的合成。一种来自 D-核糖内酯的新型 C 核苷。 | Kabat, MM., et al. 1988. Chem Pharm Bull (Tokyo). 36: 634-40. PMID: 3136937
- 利用气相色谱-串联质谱联用 QuEChERs 对 201 种农药进行全面分析--适用于不同草药品种。 | Fu, Y., et al. 2019. J Chromatogr B Analyt Technol Biomed Life Sci. 1125: 121730. PMID: 31374421
- 在气相色谱-质谱/质谱(GC-MS/MS)中使用夹层进样和分析物保护剂来减少括号校准间基质效应引起的漂移:一项案例研究。 | Soliman, M. 2021. Talanta. 225: 121970. PMID: 33592804
- 在金/Al2O3 和 SO42-/Al2O3 催化剂上从天然 D-糖绿色合成 1,5-二脱氧-1,5-亚氨基-核糖醇和 1,5-二脱氧-1,5-亚氨基-DL-阿拉伯糖醇。 | Gao, H. and Fan, A. 2021. Sci Rep. 11: 16928. PMID: 34413372
- 具有γ-烷基-γ-内酯结构的具有光学活性的信息素和芳香剂的简便通用入门。对一些戊糖†内酯衍生物的研究 | and J. Cardellach, J. Font, R. M. Ortuño.: March/April 1984. Journal of heterocyclic chemistry. Volume21, Issue2: Pages 327-331.
- 从 D-核糖酸内酯立体控制合成 6-epi-trehazolin 和 6-epi-trehalamine | Masao Shiozaki, Masami Arai, Yoshiyuki Kobayashi, Atsushi Kasuya, Shuichi Miyamoto, Youji Furukawa, Tomoko Takayama, and Hideyuki Haruyama. 1994. J. Org. Chem. 59: 4450-4460.
- 一种受保护的 L -Lyxonolactone 衍生物的简明, 高效和生产规模的合成方法L -Lyxonolactone 衍生物:一种重要的杏仁内酯核心 | Hitesh Batra, Robert M. Moriarty, Raju Penmasta, Vijay Sharma, Gabriela Stanciuc, James P. Staszewski, and Sudersan M. Tuladhar, and David A. Walsh. 2006. Organic Process Research & Development. 10: 484−486.
- α-和β-假尿苷的高度立体控制和高效合成 | Stephen Hanessian* and Roger Machaalan. 3 November 2003. Tetrahedron Letters Issue 45. Volume 44: Pages 8321-8323.
- 基于核糖内酯的 1′-碳取代胸腺嘧啶核糖核苷的合成方法 | Hiroyuki Hayakawa, et al. 1994 - Issue 1-3. Nucleosides and Nucleotides. Volume 13,: 297-308.
- 从 D-核糖内酯合成糖类。II.D-赤藓糖的另一种合成方法 | Ramesh H. Shah. Received 09 Sep 1985, Accepted 06 Dec 1985, Published online: 21 May 2008. Journal of Carbohydrate Chemistry. Volume 5, 1986 - Issue 1: Pages 139-146.
的基质:
beta-Galactosidase.订购信息
| 产品名称 | 产品编号 | 规格 | 价格 | 数量 | 收藏夹 | |
D-Ribonolactone, 5 g | sc-221517 | 5 g | $169.00 |
