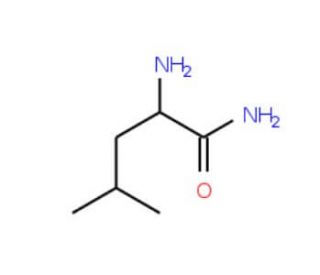
D-Leucine amide (CAS 15893-47-7)
LINKS RÁPIDOS
A D-Leucina amida é aplicada em química bioquímica, particularmente em estudos centrados na estrutura e estabilidade dos péptidos. A amida de D-leucina é fundamental para explorar as propriedades dos péptidos que incorporam D-aminoácidos, o que pode ter implicações para a compreensão da dobragem e da má dobragem das proteínas. Em enzimologia, a amida D-leucina serve como substrato ou inibidor em ensaios concebidos para caraterizar a especificidade e o mecanismo de ação das peptidases e outras enzimas que interagem com D-aminoácidos. A amida de D-leucina é utilizada no desenvolvimento de materiais à base de péptidos, em que a incorporação de D-aminoácidos pode aumentar a estabilidade contra a degradação enzimática. A D-Leucina amida está a ser estudada para compreender o papel dos D-aminoácidos na sinalização celular e nos processos neurológicos.
D-Leucine amide (CAS 15893-47-7) Referencias
- Novos desenvolvimentos na síntese de aminoácidos naturais e não naturais. | Kamphuis, J., et al. 1992. Ann N Y Acad Sci. 672: 510-27. PMID: 1476387
- Purificação, caraterização, clonagem de genes e sequenciação de nucleótidos da D: -stereospecific amino acid amidase da bactéria do solo: Delftia acidovorans. | Hongpattarakere, T., et al. 2005. J Ind Microbiol Biotechnol. 32: 567-76. PMID: 15959727
- Síntese orgânica baseada na estrutura de híbridos não naturais de aeruginosina como potentes inibidores da trombina. | Hanessian, S., et al. 2007. Bioorg Med Chem Lett. 17: 3480-5. PMID: 17428662
- Novo método enzimático de síntese de aminoácidos quirais por resolução cinética dinâmica de amidas de aminoácidos: utilização de amidases de aminoácidos estereosselectivas na presença de alfa-amino-epsilon-caprolactama racemase. | Yamaguchi, S., et al. 2007. Appl Environ Microbiol. 73: 5370-3. PMID: 17586677
- alfa,alfa-Aminoácidos cíclicos como estruturas úteis para a preparação de antagonistas dos receptores hNK(2). | Sisto, A., et al. 2007. Bioorg Med Chem Lett. 17: 4841-4. PMID: 17604625
- Uma nova aminoácido amidase D-específica de Ochrobactrum anthropi. | Asano, Y., et al. 1989. Biochem Biophys Res Commun. 162: 470-4. PMID: 2751665
- Propriedades de uma nova aminopeptidase D-específica de Ochrobactrum anthropi. | Asano, Y., et al. 1989. J Biol Chem. 264: 14233-9. PMID: 2760064
- Produção biocatalítica de (S)-2-aminobutanamida por uma nova d-aminopeptidase de Brucella sp. com elevada atividade e enantioselectividade. | Tang, XL., et al. 2018. J Biotechnol. 266: 20-26. PMID: 29217400
- Microcistinas Contendo Resíduos de Tirosina Duplamente Homologados de um Bloom de Microcystis aeruginosa: Estruturas e Citotoxicidade. | He, H., et al. 2018. J Nat Prod. 81: 1368-1375. PMID: 29847132
- Leucina aminopeptidase de lente de bovino. Estudos cinéticos com substratos e inibidores semelhantes a substratos. | Fittkau, S., et al. 1974. Eur J Biochem. 44: 523-8. PMID: 4838681
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
D-Leucine amide, 1 g | sc-285370 | 1 g | $66.00 | |||
D-Leucine amide, 5 g | sc-285370A | 5 g | $275.00 |
