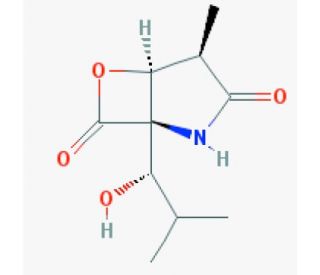
clasto-Lactacystin β-lactone (CAS 155975-72-7)
Veja citações de produtos (1)
LINKS RÁPIDOS
A clasto-lactacistina β-lactona (CAS: 155975-72-7) é um produto químico de interesse significativo, principalmente devido ao seu papel como precursor da lactacistina, uma molécula intrigante na investigação bioquímica pela sua capacidade de modular a atividade do proteassoma. A própria clasto-lactacistina β-lactona, quando metabolizada, transforma-se em lactacistina, que subsequentemente interage com o proteassoma, um complexo proteico responsável pela degradação de proteínas indesejadas ou mal dobradas nas células. A ação específica da clasto-lactacistina β-lactona envolve a sua conversão em clasto-lactacistina dihidroxiácido na presença de nucleófilos celulares, que depois inibe a atividade proteasomal, visando especificamente as subunidades β proteolíticas no núcleo 20S do proteassoma. Esta inibição é crucial para o estudo dos mecanismos de degradação das proteínas em várias condições fisiológicas, fornecendo assim informações sobre a regulação da renovação das proteínas e as suas implicações nas funções celulares. Os investigadores utilizam a clasto-lactacistina β-lactona para explorar a dinâmica da inibição do proteassoma e o seu impacto na homeostase das proteínas nas células.
clasto-Lactacystin β-lactone (CAS 155975-72-7) Referencias
- Crescimento de neurites em células PC12. Distinguir os papéis da ubiquitinação e da proteólise dependente da ubiquitina. | Obin, M., et al. 1999. J Biol Chem. 274: 11789-95. PMID: 10206996
- Uma nova via sintética enantioselectiva para análogos da omuralida com potencial para seletividade de espécies na inibição do proteassoma. | Crane, SN. and Corey, EJ. 2001. Org Lett. 3: 1395-7. PMID: 11348243
- Inibidores do proteassoma: de instrumentos de investigação a candidatos a medicamentos. | Kisselev, AF. and Goldberg, AL. 2001. Chem Biol. 8: 739-58. PMID: 11514224
- Sínteses enantioespecíficas simples dos C(2)-diastereómeros da omuralida e da 3-metilomuralida. | Reddy, LR., et al. 2005. Org Lett. 7: 2703-5. PMID: 15957926
- Inibição do proteasoma por um beta-lactâmico totalmente sintético relacionado com a salinosporamida A e a omuralida. | Hogan, PC. and Corey, EJ. 2005. J Am Chem Soc. 127: 15386-7. PMID: 16262399
- Previsão do mecanismo de ação da omuralida (clasto-lactacistina beta-lactona) na catepsina A humana com base num modelo estrutural do complexo proteasoma beta5/PRE2-subunidade/omuralida da levedura. | Aikawa, S., et al. 2006. Biochim Biophys Acta. 1764: 1372-80. PMID: 16870514
- Nova entrada para isocianetos conversíveis para a reação de Ugi e sua aplicação à síntese total formal estereocontrolada do inibidor do proteassoma omuralida. | Gilley, CB., et al. 2007. Org Lett. 9: 3631-4. PMID: 17672474
- Síntese total estereoespecífica dos inibidores do proteassoma omuralida e lactacistina. | Gu, W. and Silverman, RB. 2011. J Org Chem. 76: 8287-93. PMID: 21916437
- Omuralida e vibralactona: as diferenças na estrutura de ligação do proteassoma-β-lactona-γ-lactama alteram as preferências dos alvos. | List, A., et al. 2014. Angew Chem Int Ed Engl. 53: 571-4. PMID: 24285701
- Acesso estereocontrolado a δ-lactonas fundidas com γ-lactamas com estereocentros quaternários benzílicos angulares. | Beng, TK., et al. 2022. RSC Adv. 12: 17617-17620. PMID: 35765420
- Inibição das actividades do proteassoma e modificação amino-terminal da treonina específica da subunidade pela lactacistina. | Fenteany, G., et al. 1995. Science. 268: 726-31. PMID: 7732382
- Estudos mecanísticos sobre a inativação do proteasoma pela lactacistina em células em cultura. | Dick, LR., et al. 1997. J Biol Chem. 272: 182-8. PMID: 8995245
- Síntese total e atividade biológica da lactacistina, omuralida e análogos. | Corey, EJ. and Li, WD. 1999. Chem Pharm Bull (Tokyo). 47: 1-10. PMID: 9987821
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
clasto-Lactacystin β-lactone, 100 µg | sc-202106 | 100 µg | $254.00 |
