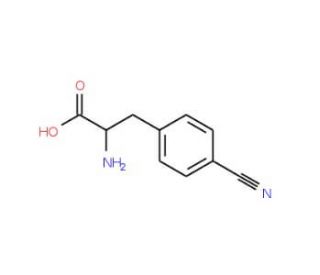
4-Cyano-L-phenylalanine (CAS 104531-20-6)
LINKS RÁPIDOS
A 4-Cyano-L-fenilalanina é um derivado de aminoácido e pertence à classe dos aminoácidos aromáticos. A 4-Cyano-L-fenilalanina é caracterizada pela presença de um grupo ciano (CN) ligado à molécula de fenilalanina. Na pesquisa científica, a 4-Cyano-L-fenilalanina encontra várias aplicações devido às suas propriedades químicas exclusivas. Normalmente, é usada como um bloco de construção ou precursor na síntese de peptídeos e na descoberta de medicamentos. O grupo ciano pode servir como um grupo funcional versátil, permitindo a introdução de diversas modificações químicas e criando análogos de peptídeos com atividades biológicas alteradas. Uma das principais aplicações da 4-Cyano-L-fenilalanina é no campo da química medicinal. Os pesquisadores utilizam esse composto para desenvolver novos peptídeos com bioatividade, estabilidade ou propriedades farmacocinéticas aprimoradas. Ao incorporar a 4-Cyano-L-phenylalanine em sequências de peptídeos, os cientistas podem modular as interações do peptídeo com alvos biológicos, como receptores ou enzimas, o que pode levar a uma maior eficácia terapêutica. O mecanismo de ação da 4-Cyano-L-phenylalanine depende do contexto específico e do peptídeo ou molécula em que ela está incorporada. Como um derivado de aminoácido, a 4-Ciano-L-fenilalanina pode participar da formação de ligações peptídicas durante a síntese, contribuindo para a estrutura geral e a função do peptídeo resultante. A presença do grupo ciano pode influenciar as interações do peptídeo com alvos biológicos, alterando sua conformação, estabilidade ou afinidade de ligação ao receptor. Além disso, o grupo ciano pode sofrer reações químicas, o que permite outras modificações ou funcionalizações do peptídeo. Essas modificações podem afetar a solubilidade do peptídeo, a permeabilidade da membrana ou a estabilidade metabólica, influenciando seu comportamento em sistemas biológicos.
4-Cyano-L-phenylalanine (CAS 104531-20-6) Referencias
- Novos substratos cromogénicos da catepsina G de neutrófilos humanos com resíduos de aminoácidos aromáticos não naturais na posição P(1) selecionados por métodos de química combinatória. | Wysocka, M., et al. 2007. Mol Divers. 11: 93-9. PMID: 17653609
- Expansão da utilidade da 4-ciano-L-fenilalanina como um repórter vibracional de ambientes proteicos. | Bazewicz, CG., et al. 2012. J Phys Chem B. 116: 10824-31. PMID: 22909326
- Conceção racional de uma proteína de ligação à ftalocianina de zinco. | Mutter, AC., et al. 2014. J Struct Biol. 185: 178-85. PMID: 23827257
- Sonda vibracional sensível, específica do local e estável dos ambientes locais das proteínas: 4-azidometil-L-fenilalanina. | Bazewicz, CG., et al. 2013. J Phys Chem B. 117: 8987-93. PMID: 23865850
- O papel de 'guardião' do Trp222 determina a enantiopreferência da dicetoredutase em relação à 2-cloro-1-feniletanona. | Ma, H., et al. 2014. PLoS One. 9: e103792. PMID: 25072248
- Isolamento e Diversificação Sintética da Jadomicina 4-Amino-l-fenilalanina. | Martinez-Farina, CF., et al. 2015. J Nat Prod. 78: 1208-14. PMID: 26035093
- Incorporação melhorada de aminoácidos não canónicos por um supressor de tRNA (Tyr) concebido. | Rauch, BJ., et al. 2016. Biochemistry. 55: 618-28. PMID: 26694948
- Sondagem da eficácia do repórter espetroscópico de aminoácidos não naturais: um estudo estrutural. | Dippel, AB., et al. 2016. Acta Crystallogr D Struct Biol. 72: 121-30. PMID: 26894540
- Comparação de cromóforos biológicos: propriedades fotofísicas de derivados de cianofenilalanina. | Martin, JP., et al. 2016. Phys Chem Chem Phys. 18: 20750-7. PMID: 27412819
- Sondas minimalistas de infravermelhos e de fluorescência da função das proteínas. | Gosavi, PM. and Korendovych, IV. 2016. Curr Opin Chem Biol. 34: 103-109. PMID: 27599185
- Exploração dos ambientes locais de solvatação de uma proteína heme utilizando o repórter espetroscópico 4-ciano-l-fenilalanina. | Kearney, C., et al. 2018. RSC Adv. 8: 13503-13512. PMID: 29780583
- Estruturas cristalinas da proteína fluorescente verde com o aminoácido não natural 4-nitro-L-fenilalanina. | Maurici, N., et al. 2018. Acta Crystallogr F Struct Biol Commun. 74: 650-655. PMID: 30279317
- Investigação estrutural e espectrofotométrica de dois cromóforos não naturais alterados por aminoácidos na proteína fluorescente verde superfolder. | Olenginski, GM., et al. 2021. Acta Crystallogr D Struct Biol. 77: 1010-1018. PMID: 34342274
- Peptídeos concebidos de novo para entrega celular e localização subcelular. | Rhys, GG., et al. 2022. Nat Chem Biol. 18: 999-1004. PMID: 35836017
- Desvendando ambientes locais complexos de proteínas com 4-Cyano-l-fenilalanina. | Lee, B., et al. 2022. J Phys Chem B. 126: 8957-8969. PMID: 36317866
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
4-Cyano-L-phenylalanine, 1 g | sc-290253 | 1 g | $156.00 | |||
4-Cyano-L-phenylalanine, 5 g | sc-290253A | 5 g | $604.00 |
