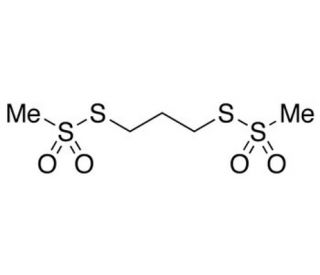
1,3-Propanediyl Bismethanethiosulfonate (CAS 55-96-9)
LINKS RÁPIDOS
O 1,3-propanodiil bismetanosulfonato é um reticulador químico que contém dois grupos reativos de metanotiossulfonato, que podem formar ligações dissulfeto com moléculas que contêm tiol. Esse composto é amplamente usado em pesquisas bioquímicas para estudar interações proteína-proteína, pois pode ligar covalentemente resíduos de cisteína em moléculas de proteína adjacentes. Com o uso do 1,3-propanodiil bismetanotiossulfonato, os pesquisadores podem estabilizar complexos proteicos transitórios ou fracos, facilitando sua caracterização estrutural e funcional por meio de técnicas como cristalografia de raios X e espectrometria de massa. Além disso, ele é empregado na investigação de alterações conformacionais em proteínas, já que a formação de ligações dissulfeto pode bloquear as proteínas em conformações específicas. Sua utilidade também se estende ao projeto de novos biomateriais, onde pode ser usado para introduzir ligações cruzadas e aumentar a estabilidade de materiais à base de proteínas. Além disso, esse reticulador auxilia no desenvolvimento de ensaios para monitorar o estado redox das proteínas, uma vez que as ligações dissulfeto que ele forma podem ser reduzidas, proporcionando uma modificação reversível que pode refletir mudanças no ambiente redox celular.
1,3-Propanediyl Bismethanethiosulfonate (CAS 55-96-9) Referencias
- Determinação das dimensões do domínio de ligação a fármacos da glicoproteína-P humana utilizando compostos de ligação cruzada de tiol como réguas moleculares. | Loo, TW. and Clarke, DM. 2001. J Biol Chem. 276: 36877-80. PMID: 11518701
- O aprisionamento de nucleótidos por vanadato nos locais de ligação ao ATP da glicoproteína-P humana resistente a múltiplos fármacos expõe diferentes resíduos ao local de ligação ao fármaco. | Loo, TW. and Clarke, DM. 2002. Proc Natl Acad Sci U S A. 99: 3511-6. PMID: 11891276
- Posições expostas à superfície nas hélices transmembranares da permease da lactose de Escherichia coli determinadas por reticulação intermolecular de tiol. | Guan, L., et al. 2002. Proc Natl Acad Sci U S A. 99: 3475-80. PMID: 11904412
- Empacotamento em hélice do trocador Na+-Ca2+ cardíaco: proximidade dos segmentos transmembranares 1, 2 e 6. | Ren, X., et al. 2006. J Biol Chem. 281: 22808-14. PMID: 16785232
- Sondagem da estrutura da proteína de membrana dimérica KtrB. | Albright, RA., et al. 2007. J Biol Chem. 282: 35046-55. PMID: 17932047
- Estequiometria da subunidade dimérica do canal de prótons dependente de voltagem humano Hv1. | Lee, SY., et al. 2008. Proc Natl Acad Sci U S A. 105: 7692-5. PMID: 18509058
- Múltiplos contactos entre os domínios membranar e citoplasmático no regulador de condutância transmembranar da fibrose cística (CFTR) medeiam a regulação da abertura do canal. | He, L., et al. 2008. J Biol Chem. 283: 26383-90. PMID: 18658148
- Análise estrutural da entrada extracelular da via de permeação do transportador de serotonina. | Torres-Altoro, MI., et al. 2010. J Biol Chem. 285: 15369-15379. PMID: 20304925
- Oligomerização do canal de protões controlado por voltagem. | Musset, B., et al. 2010. Channels (Austin). 4: 260-5. PMID: 20676047
- A topologia do trocador de Na⁺/Ca²⁺ cardíaco, NCX1. | Ren, X. and Philipson, KD. 2013. J Mol Cell Cardiol. 57: 68-71. PMID: 23376057
- O fosfatidilglicerol dirige a ligação e a ação inibitória da proteína EIIAGlc no transportador de maltose. | Bao, H. and Duong, F. 2013. J Biol Chem. 288: 23666-74. PMID: 23821551
- A restrição da hélice lateral do complexo respiratório I através de ligações cruzadas não prejudica a atividade enzimática ou a translocação de protões. | Zhu, S. and Vik, SB. 2015. J Biol Chem. 290: 20761-20773. PMID: 26134569
- A perda de atividade do Complexo I na enzima de Escherichia coli resulta do truncamento do terminal C da subunidade K, mas não da sua ligação cruzada às subunidades N ou L. | Zhu, S., et al. 2016. J Bioenerg Biomembr. 48: 325-33. PMID: 26931547
- Dinâmica do laço D e estrutura crio-EM de resolução quase atómica da F-Actina ligada à faloidina. | Das, S., et al. 2020. Structure. 28: 586-593.e3. PMID: 32348747
- Análise estrutural da proteína alvo pelo método de acessibilidade à cisteína substituída. | Cai, T. and Tomita, T. 2018. Bio Protoc. 8: e2470. PMID: 34395783
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
1,3-Propanediyl Bismethanethiosulfonate, 25 mg | sc-208779 | 25 mg | $379.00 |
