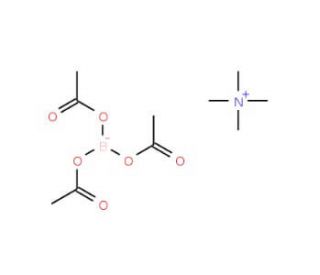
Tetramethylammonium triacetoxyborohydride 的分子结构, CAS编号: 109704-53-2
Tetramethylammonium triacetoxyborohydride (CAS 109704-53-2)
CAS号码:
109704-53-2
分子量:
263.10
分子式:
C10H22BNO6
补充资料:
此类物品属于危险品,运输时可能需要支付额外运费。
仅供科研使用。不可用于诊断或治疗。
* 参考分析证明 大量特定数据 (包括水 含量).
快捷链接
订购信息
描述
技术信息
安全信息
安全技术说明书和分析证明书
三乙酸基四甲基硼氢化铵(TMAB)是一种在合成有机化学领域广泛使用的强效有机化合物。它是一种强有力的还原剂,主要用于将醛和酮转化为相应的醇。除了这一作用外,三乙酸基四甲基硼氢化铵在构建胺、酯和酰胺等不同有机分子中起着关键作用。在合成有机化学中,三乙酸基四甲基硼氢化铵的广泛使用是显而易见的。它的部署包括创造无数有机实体,从胺、酯和酰胺到聚合物、染料。三乙酸基四甲基硼氢化铵作为强效还原剂的能力是毋庸置疑的,特别是它将醛和酮转化为相应醇的能力。这种转变的潜在机制涉及电子从硼原子到醛或酮的羰基部分的精心编排的转移,最终导致羰基还原为醇。
Tetramethylammonium triacetoxyborohydride (CAS 109704-53-2) 参考文献
- 利用共轭烯丙基化作用安装 C-1 季碳,对 (-)-FR901483 进行合成研究。 | Gotchev, DB. and Comins, DL. 2006. J Org Chem. 71: 9393-402. PMID: 17137366
- 以原子经济学方法立体选择性合成金合欢素的环 a 和 B 亚基。 | Trost, BM., et al. 2011. Chemistry. 17: 9777-88. PMID: 21774000
- 开发 (-)-kinamycin F 和 (-)-lomaiviticin aglycon 的对映体选择性合成路线。 | Woo, CM., et al. 2012. J Am Chem Soc. 134: 17262-73. PMID: 23030272
- 钯催化炔基取代中的立体控制:通过动力学解析得到对映体的 1,5-炔和丙炔基乙酸酯。 | Ardolino, MJ., et al. 2013. Adv Synth Catal. 355: 3413-3419. PMID: 24839434
- 结核分枝杆菌 PapA5 在合成烷基 β-二醇脂过程中的二酰转移酶活性和链长特异性 | Touchette, MH., et al. 2015. Biochemistry. 54: 5457-68. PMID: 26271001
- 合成一种简化的儿茶酚胺 A 的三唑类似物。 | Hemi Cumming, A., et al. 2016. Org Biomol Chem. 14: 5117-27. PMID: 27180995
- 通过基于药理的虚拟筛选, 分子对接和生物测定鉴定新型乙酰胆碱酯酶抑制剂。 | Jang, C., et al. 2018. Sci Rep. 8: 14921. PMID: 30297729
- 在大肠杆菌中,用于工程化 preQ1 核糖开关的叠氮功能配体的细胞活性优于氨基功能配体。 | Neuner, E., et al. 2018. RNA Biol. 15: 1376-1383. PMID: 30332908
- Xiamycins A, C, F, H 和 Oridamycin A 的全合成及其抗真菌性能的初步评估。 | Pfaffenbach, M., et al. 2019. Angew Chem Int Ed Engl. 58: 15304-15308. PMID: 31419367
- 简单合成柴胡皂苷。 | Wang, Z., et al. 2021. Molecules. 26: PMID: 33808330
订购信息
| 产品名称 | 产品编号 | 规格 | 价格 | 数量 | 收藏夹 | |
Tetramethylammonium triacetoxyborohydride, 10 g | sc-258237 | 10 g | $203.00 |
