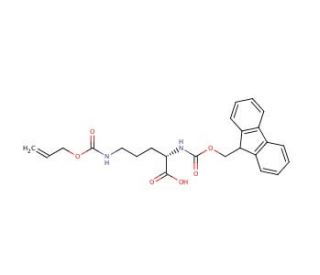
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7)
LINKS RÁPIDOS
O Fmoc-Orn(Alloc)-OH representa um derivado do aminoácido Ornitina, que ocorre naturalmente e participa no metabolismo do azoto como intermediário no ciclo da ureia. Amplamente utilizado em síntese orgânica e bioquímica, este derivado de aminoácido possui uma versatilidade significativa. Serve para vários fins, incluindo a síntese de proteínas e péptidos, bem como para servir de material de partida para a síntese de vários compostos. Na investigação científica, o Fmoc-Orn(Alloc)-OH encontra aplicações extensivas, particularmente na síntese de péptidos e na síntese de proteínas. A sua utilidade reside na introdução de diversos grupos funcionais em péptidos e proteínas. Além disso, este composto é utilizado na síntese de outros compostos, como pequenas moléculas e polímeros. A sua capacidade de introduzir uma vasta gama de grupos funcionais nestes compostos é altamente vantajosa. O mecanismo de ação do Fmoc-Orn(Alloc)-OH depende da sua reatividade com aminoácidos e outras moléculas. Através da sua interação com um aminoácido, forma uma ligação covalente conhecida como ligação peptídica, facilitando a ligação de aminoácidos para criar péptidos e proteínas. Além disso, o Fmoc-Orn(Alloc)-OH pode estabelecer ligações covalentes com pequenas moléculas e polímeros através das suas reacções com eles.
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7) Referencias
- Síntese e produção de anticorpos específicos para glicopeptídeos com N-GlcNAcilação de arginina. | Pan, M., et al. 2014. Angew Chem Int Ed Engl. 53: 14517-21. PMID: 25353391
- Deteção específica por espetrometria de massa em tandem de resíduos de arginina modificados por AGE em péptidos. | Schmidt, R., et al. 2015. J Mass Spectrom. 50: 613-24. PMID: 25800199
- Deteção selectiva de pirofosfato em meios fisiológicos utilizando peptídeos de zinco(II)dipicolilamino-funcionalizados. | Zwicker, VE., et al. 2015. Org Biomol Chem. 13: 7822-9. PMID: 26107804
- Peptídeos sintéticos que imitam o local de ligação da acetilcolinesterase humana ao seu inibidor fasciculina 2. | Kafurke, U., et al. 2015. J Pept Sci. 21: 723-30. PMID: 26200472
- A resolução da ligação α-glicosídica do fator de alongamento da tradução P arginina-ramnosilado desencadeia a geração do primeiro anticorpo específico ArgRha. | Li, X., et al. 2016. Chem Sci. 7: 6995-7001. PMID: 28451135
- Reconhecimento de Análogos de Dimetilarginina pela Proteína Spindlin1 com Domínio Tudor em Tandem. | Porzberg, MRB., et al. 2022. Molecules. 27: PMID: 35164245
- Geração biocompatível e selectiva de péptidos bicíclicos. | Ullrich, S., et al. 2022. Angew Chem Int Ed Engl. 61: e202208400. PMID: 35852030
- Péptidos peguilados. II. Síntese em fase sólida de péptidos peguilados com amino, carboxi e cadeias laterais. | Lu, YA. and Felix, AM. 1994. Int J Pept Protein Res. 43: 127-38. PMID: 8200730
- Um papel duplo do ácido fenilborónico como recetor de hidratos de carbono e como supressor do fluoróforo pireno vizinho | Lok Nath Neupane, Chuda Raj Lohani, Jeongho Kim, Keun-Hyeung Lee. 2013. Tetrahedron. 69: 11057-11063.
- Síntese total do domínio de morte TRADD com N-GlcNAcilação da arginina por ligação química nativa à base de hidrazida | Ye Wu a b 1, Yulei Li c 1, Wei Cong a, Yan Zou b, Xiang Li b, Honggang Hu a. 2020. Chinese Chemical Letters. 31: 107-110.
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Fmoc-Orn(Alloc)-OH, 5 g | sc-235198 | 5 g | $153.00 |
