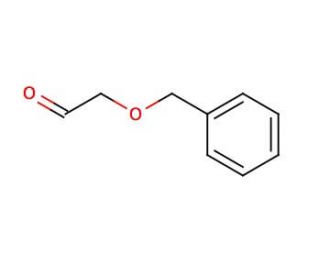
2-(Benzyloxy)acetaldehyde の分子構造、CAS番号: 60656-87-3
2-(Benzyloxy)acetaldehyde (CAS 60656-87-3)
アプリケーション:
CAS 番号:
60656-87-3
純度:
97%
分子量:
150.17
分子式:
C9H10O2
試験・研究用以外には使用しないでください。 臨床及び体外診断には使用できません。
* Refer to Certificate of Analysis for lot specific data.
クイックリンク
注文情報
説明
技術サポート情報
安全情報
SDSと分析証明書
2‐ (ベンジルオキシ) アセトアルデヒドは,その官能基により種々の合成経路の中間体となるため,有機化学研究に用いられる化合物である。複素環化合物の形成や、アルドールやその他の炭素-炭素結合形成反応におけるアルデヒド成分としてしばしば用いられる。ベンジルオキシ部分は、特定の条件下で除去可能な保護基として機能し、選択的変換を可能にする。2- (ベンジルオキシ) アセトアルデヒドに関する研究では、標的分子の収率と選択性を高めるための反応条件の最適化に焦点が当てられることが多い。さらに,この化合物は化学反応性の機構を研究し,新しい合成方法論を開発するために使用される。種々の反応条件下でのその安定性と分子構造に複雑性を導入する能力は,合成有機化学における2‐ (ベンジルオキシ) アセトアルデヒドの有用性を拡張するために通常探求される側面である。
2-(Benzyloxy)acetaldehyde (CAS 60656-87-3) 参考文献
- ジソラゾールA(1)およびC(1)の全合成に向けて:マスクされた南側セグメントの不斉合成。 | Hartung, IV., et al. 2002. Org Lett. 4: 3239-42. PMID: 12227758
- C型肝炎ウイルスRNA複製阻害剤としての光学的に純粋なジオキソランの合成と評価。 | Bera, S., et al. 2003. Bioorg Med Chem Lett. 13: 4455-8. PMID: 14643345
- キラルなアゼチジンヌクレオシド類似体の合成を目指した分子内1,3-双極性付加環化反応:D-グルコの場合。 | Pádár, P., et al. 2005. Nucleosides Nucleotides Nucleic Acids. 24: 743-5. PMID: 16248028
- オメガ不飽和ニトロンの分子内1,3-双極性付加環化反応によるポリヒドロキシル化9-オキサ-1-アザビシクロ[4.2.1]ノナンの単一ジアステレオマー。 | Padar, P., et al. 2006. J Org Chem. 71: 8669-72. PMID: 17064056
- VGFおよびPGP9.5のプロモーターメチル化と卵巣癌の進行との関連。 | Brait, M., et al. 2013. PLoS One. 8: e70878. PMID: 24086249
- 高エナンチオマー純度のd-[1-(14) C]-セリンの短時間合成。 | Song, F., et al. 2015. J Labelled Comp Radiopharm. 58: 173-6. PMID: 25728900
- アクマトヴィッチ反応とその生物活性分子合成への応用。 | Ghosh, AK. and Brindisi, M. 2016. RSC Adv. 6: 111564-111598. PMID: 28944049
- 2-ベンジルオキシアルデヒドを用いたインドールからα-(3-インドリル)ケトンへのブレンステッド酸触媒カスケード反応。 | Banerjee, A. and Maji, MS. 2019. Chemistry. 25: 11521-11527. PMID: 31283058
- 複雑な天然物の全合成における骨格と官能基のバランス:チグリアン, ダフナン, インゲナンジテルペノイドのケーススタディ。 | Liu, Z., et al. 2021. Nat Prod Rep. 38: 1589-1617. PMID: 33508045
- プロテアーゼ阻害剤のワーヘッドとペプチドミメティック配列との適合性の検討-包括的反応性と選択性の研究-. | Müller, P., et al. 2023. Int J Mol Sci. 24: PMID: 37108388
注文情報
| 製品名 | カタログ # | 単位 | 価格 | 数量 | お気に入り | |
2-(Benzyloxy)acetaldehyde, 1 g | sc-208936 | 1 g | $93.00 |
