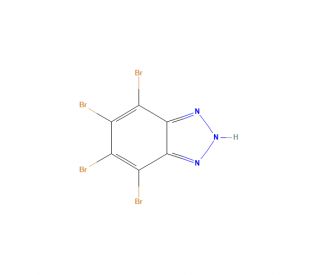
TBB (CAS 17374-26-4)
参考文献をチェックします (17)
クイックリンク
TBB(4,5,6,7-テトラブロモベンゾトリアゾール)は、さまざまな科学研究に広く用いられている有機化合物である。TBBTはベンゾトリアゾールのコアに4個の臭素原子が結合した芳香族化合物である。光や熱による劣化に対して安定であるため、様々な研究に最適である。この結晶性の白色固体は、細胞透過性のベンゾトリアゾロ化合物で、ATP/GTP結合部位に競合的に結合することにより、プロテインキナーゼを選択的に阻害する能力で有名である。具体的には、カゼインキナーゼIIα(CK2α)および二重特異性チロシン(Y)リン酸化調節キナーゼ1A(Dyrk1A)に対して強力な阻害作用を示す。TBBの強い結合力は、疎水性相互作用とファンデルワールス相互作用の両方によるものである。グリコーゲン合成酵素キナーゼ(GSK)、サイクリン依存性キナーゼ2(CDK2)、ホスホリラーゼキナーゼなどのキナーゼに対する阻害作用は少ないが、C型肝炎ウイルスやウエストナイルウイルスのNS3関連ウイルスヘリカーゼ活性に対する阻害作用を示した。さらに、TBBはJurkat細胞のアポトーシス誘導剤としても使用されている。さらに、TBBはシクロオキシゲナーゼ(COX)酵素の阻害剤として作用すると推測されている。COX酵素はプロスタグランジンの合成に関与しており、炎症、疼痛調節、その他の生理学的反応などのプロセスにおいて重要な役割を果たしている。COX活性を阻害することにより、TBBはプロスタグランジンの産生を効果的に減少させることができ、特定の病態に治療効果をもたらす可能性がある。このように、TBBは細胞増殖、分化、免疫系機能への影響を研究する多くのin vitro研究で有用性を見出している。また、中枢神経系への影響やがん治療への応用の可能性についても幅広く研究されている。
TBB (CAS 17374-26-4) 参考文献
- プロテインキナーゼCK2(カゼインキナーゼ-2)のATP部位特異的阻害剤, 4,5,6,7-テトラブロモベンゾトリアゾールの選択性。 | Sarno, S., et al. 2001. FEBS Lett. 496: 44-8. PMID: 11343704
- プロテインキナーゼCK2阻害剤4,5,6,7-テトラブロモベンゾトリアゾール(TBB)は, Jurkat細胞においてアポトーシスとカスパーゼ依存的な造血系細胞特異的タンパク質1(HS1)の分解を誘導する。 | Ruzzene, M., et al. 2002. Biochem J. 364: 41-7. PMID: 11988074
- C型肝炎ウイルスおよび関連ウイルスのNTPase/ヘリカーゼ活性阻害剤としてのハロゲン化ベンズイミダゾールおよびベンゾトリアゾール。 | Borowski, P., et al. 2003. Eur J Biochem. 270: 1645-53. PMID: 12694177
- 4,5,6,7-テトラブロモベンズイミダゾールのATP競合的強力阻害剤としての選択性。 | Zień, P., et al. 2003. Biochem Biophys Res Commun. 306: 129-33. PMID: 12788077
- 5-oxo-5,6-dihydroindolo-(1,2-a)quinazolin-7-yl]acetic acid (IQA)によるプロテインキナーゼCK2の特異的阻害に関する生化学的および3次元構造学的研究。 | Sarno, S., et al. 2003. Biochem J. 374: 639-46. PMID: 12816539
- 4,5,6,7-テトラブロモベンズイミダゾール由来のプロテインキナーゼCK2阻害剤の最適化。 | Pagano, MA., et al. 2004. J Med Chem. 47: 6239-47. PMID: 15566294
- ケモプロテオミクスによるCK2阻害剤の偏りのない評価:CK2に対する阻害剤効果の特徴づけと新規阻害剤標的の同定。 | Duncan, JS., et al. 2008. Mol Cell Proteomics. 7: 1077-88. PMID: 18258654
- プロテインキナーゼCK2の新しい阻害剤, ベンズイミダゾールとベンゾトリアゾールの類似体。 | Bretner, M., et al. 2008. Mol Cell Biochem. 316: 87-9. PMID: 18548199
- テトラブロモベンゾトリアゾールおよびいくつかのC5置換類似体によるヒトプロテインキナーゼCK2αの阻害におけるハロゲン結合と疎水性相互作用の相対的役割。 | Wasik, R., et al. 2010. J Phys Chem B. 114: 10601-11. PMID: 20734498
- CK2阻害は小胞体ストレス応答を介してアポトーシスを誘導する。 | Hessenauer, A., et al. 2011. Cell Signal. 23: 145-51. PMID: 20807566
- CK2はAP-2αをリン酸化し, その転写活性を増加させる。 | Ren, K., et al. 2011. BMB Rep. 44: 490-5. PMID: 21777522
- CK2活性は, FGF14と電位依存性ナトリウムチャネルとの相互作用および神経細胞の興奮性に必要である。 | Hsu, WC., et al. 2016. FASEB J. 30: 2171-86. PMID: 26917740
- CK2阻害によって誘導されるPDK4-AMPK軸は, 神経膠腫における代謝適応と生存応答を制御する。 | Dixit, D., et al. 2016. Exp Cell Res. 344: 132-142. PMID: 27001465
- エボラウイルスとマールブルグウイルスのVP35コイルドコイルが三分割GFP相補体化によって抗ウイルス標的であることが確認された。 | Zinzula, L., et al. 2022. iScience. 25: 105354. PMID: 36325051
- ヒト赤血球表面糖タンパク質のポリスチレンラテックス球への吸着。 | Fromageot, HP. 1977. J Lab Clin Med. 90: 324-9. PMID: 886218
注文情報
| 製品名 | カタログ # | 単位 | 価格 | 数量 | お気に入り | |
TBB, 10 mg | sc-202830 | 10 mg | $245.00 | |||
TBB, 25 mg | sc-202830A | 25 mg | $370.00 | |||
TBB, 50 mg | sc-202830C | 50 mg | $454.00 | |||
TBB, 100 mg | sc-202830B | 100 mg | $760.00 | |||
TBB, 250 mg | sc-202830D | 250 mg | $1817.00 |
