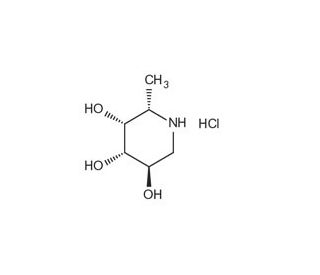
Deoxyfuconojirimycin hydrochloride (CAS 210174-73-5)
Vedere citazioni di prodotto (3)
LINK RAPIDI
La deossifuconojirimicina cloridrato, un analogo dell'iminosugar fucosio, è un composto riconosciuto per la sua azione inibitoria sugli enzimi glicosidasi. Questa inibizione è particolarmente importante nello studio dell'elaborazione e della maturazione delle glicoproteine all'interno del reticolo endoplasmatico e dell'apparato di Golgi. I ricercatori sfruttano la deossifuconojirimicina cloridrato per studiare il ruolo delle glicosidasi nel corretto ripiegamento delle glicoproteine, con implicazioni per la comprensione delle malattie caratterizzate da un errato ripiegamento delle proteine. Inoltre, questo composto è utilizzato in glicobiologia per esplorare la sintesi e la funzione dei glicolipidi e delle glicoproteine, nonché gli effetti patologici della loro sintesi aberrante. L'inibizione delle glicosidasi da parte della deossifuconojirimicina cloridrato è anche un punto di interesse nello studio della replicazione virale, dove la corretta glicosilazione delle proteine virali è essenziale per l'assemblaggio e l'infettività del virus. L'azione del composto aiuta a chiarire i complessi percorsi delle interazioni ospite-virus e la potenziale interruzione di questi processi.
Deoxyfuconojirimycin hydrochloride (CAS 210174-73-5) Referenze
- Fucosiltransferasi nello sviluppo di Schistosoma mansoni. | Marques, ET., et al. 2001. Glycobiology. 11: 249-59. PMID: 11320063
- Sintesi conveniente e valutazione dell'attività inibitoria enzimatica di diversi derivati N-alchilici, N-fenilalchilici e isourea ciclici della 5a-carba-alfa-DL-fucopiranosilammina. | Ogawa, S., et al. 2002. Bioorg Med Chem Lett. 12: 2811-4. PMID: 12270152
- Basi strutturali del meccanismo di reazione catalitica della nuova 1,2-alfa-L-fucosidasi di Bifidobacterium bifidum. | Nagae, M., et al. 2007. J Biol Chem. 282: 18497-18509. PMID: 17459873
- Le società di alfa-L-fucosio associate alla superficie cellulare modulano la progressione neoplastica del cancro al seno umano. | Yuan, K., et al. 2008. Pathol Oncol Res. 14: 145-56. PMID: 18553163
- Inibizione dell'alfa-L-fucosidasi da parte di derivati della deossifuconojirimicina e della deossimannojirimicina. | Winchester, B., et al. 1990. Biochem J. 265: 277-82. PMID: 2137330
- Ruolo delle alfa-L-fucosidasi associate allo sperma di topo nella fecondazione. | Phopin, K., et al. 2013. Mol Reprod Dev. 80: 273-85. PMID: 23426913
- Digestione dei carboidrati nelle zecche e una α-L-fucosidasi digestiva. | Moreti, R., et al. 2013. J Insect Physiol. 59: 1069-75. PMID: 23994295
- Caratterizzazione di una α-l-fucosidasi del patogeno parodontale Tannerella forsythia. | Megson, ZA., et al. 2015. Virulence. 6: 282-92. PMID: 25831954
- Un dominio lectinico di tipo F dirige l'attività della Streptosporangium roseum alfa-l-fucosidasi. | Bishnoi, R., et al. 2018. Glycobiology. 28: 860-875. PMID: 30169639
- Sviluppo di un metodo UHPLC-MS per lo screening di inibitori contro l'α-L-1,3-fucosidasi. | Liu, T., et al. 2019. Anal Bioanal Chem. 411: 1467-1477. PMID: 30706074
- Le strutture crio-EM della fucosidasi umana FucA1 rivelano informazioni sul riconoscimento del substrato e sulla catalisi. | Armstrong, Z., et al. 2022. Structure. 30: 1443-1451.e5. PMID: 35907402
- Purificazione e caratterizzazione dell'alfa-L-fucosidasi dal surnatante di colture cellulari di criceto cinese. | Gramer, MJ., et al. 1994. Glycobiology. 4: 611-6. PMID: 7881175
- Il legame degli spermatozoi bovini con l'epitelio oviduttale implica il riconoscimento del fucosio. | Lefebvre, R., et al. 1997. Biol Reprod. 56: 1198-204. PMID: 9160719
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Deoxyfuconojirimycin hydrochloride, 1 mg | sc-205644 | 1 mg | $112.00 | |||
Deoxyfuconojirimycin hydrochloride, 5 mg | sc-205644A | 5 mg | $265.00 | |||
Deoxyfuconojirimycin hydrochloride, 25 mg | sc-205644B | 25 mg | $479.00 | |||
Deoxyfuconojirimycin hydrochloride, 50 mg | sc-205644C | 50 mg | $694.00 | |||
Deoxyfuconojirimycin hydrochloride, 100 mg | sc-205644D | 100 mg | $1019.00 |
