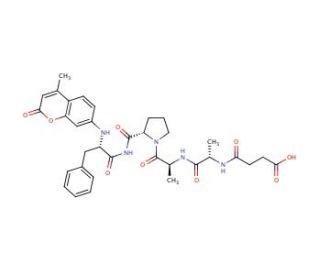
Chymotrypsin Substrate II, Fluorogenic 의 분자 구조, CAS 번호: 88467-45-2
Chymotrypsin Substrate II, Fluorogenic (CAS 88467-45-2)
대체 이름:
N-Succinyl-Ala-Ala-Pro-Phe-7-amido-4-methylcoumarin; Suc-AAPF-AMC
적용:
Chymotrypsin Substrate II, Fluorogenic 는 정량적 불소 생성 키모트립신 기질입니다.
CAS 등록번호:
88467-45-2
순도:
≥98%
분자량:
661.70
분자식:
C34H39N5O9
연구용으로만 사용가능합니다. 진단이나 치료용으로 사용불가합니다.
* Refer to Certificate of Analysis for lot specific data.
빠른 링크
주문정보
설명
기술정보
안전정보
SDS 및 분석 증명서
키모트립신 기질 II, 플루오로제닉은 티로신, 트립토판, 페닐알라닌과 같은 방향족 아미노산의 카르복실 측에서 펩티드 결합을 절단하는 소화 프로테아제인 키모트립신의 기질 역할을 하는 특수 설계된 펩티드이다. 이 기질의 플루오로제닉적 측면은 키모트립신에 의한 효소 절단 시 형광 신호를 방출하여 효소의 활성을 실시간으로 모니터링할 수 있다는 것을 의미한다. 이러한 특성 때문에 다양한 연구 및 분석 응용, 특히 프로테아제 활성 및 억제제 스크리닝 연구에 귀중한 도구가 된다. 연구자들은 기질이 절단될 때 형광 강도가 증가하는 것을 측정하여 효소의 속도, 기질 친화도(Km) 및 촉매 효율(kcat)을 측정하여 효소의 촉매 메커니즘에 대한 통찰력을 제공할 수 있다.
Chymotrypsin Substrate II, Fluorogenic (CAS 88467-45-2) 참고자료
- 사이클로필린-A가 산화 스트레스로부터 세포를 보호한다는 증거. | Doyle, V., et al. 1999. Biochem J. 341 (Pt 1): 127-32. PMID: 10377253
- 사이클로필린-A는 쥐 신경세포 B50 세포에서 흥분성 독소에 의한 카스파제 활성화에 관여합니다. | Capano, M., et al. 2002. Biochem J. 363: 29-36. PMID: 11903043
- 유도 결합 플라즈마-질량 분석법 기반 프로테아제 분석법 개발. | Lathia, US., et al. 2010. Anal Biochem. 398: 93-8. PMID: 19912984
- 인간 혈청에서 새로운 쿠니츠 유형 프로테아제 억제제의 기능적 발현 Schistosoma mansoni. | Ranasinghe, SL., et al. 2015. Parasit Vectors. 8: 408. PMID: 26238343
- 에키노코쿠스 그라눌로수스에서 두 가지 강력한 쿠니츠 유형 프로테아제 억제제의 복제 및 특성 분석. | Ranasinghe, SL., et al. 2015. PLoS Negl Trop Dis. 9: e0004268. PMID: 26645974
- 두 가지 항진균 단백질, 식물 디펜신 NaD1과 소 췌장 트립신 억제제 간의 시너지 활성. | Bleackley, MR., et al. 2017. mSphere. 2: PMID: 29062897
- 바우히니아 바우히니오이데스의 칼리크레인 억제제와 트립신 복합체의 결정 구조 및 칼리크레인 복합체 모델링. | Li, M., et al. 2019. Acta Crystallogr D Struct Biol. 75: 56-69. PMID: 30644845
- 심근 세포에 의한 키마제 흡수는 심장 용적 과부하에서 미오신 분해를 초래합니다. | Powell, PC., et al. 2019. Heliyon. 5: e01397. PMID: 30997426
- 서핀b1과 서핀b6에 의한 카텝신 G 억제는 호중구와 단핵구의 프로그램된 괴사를 방지하고 GSDMD에 의한 염증을 감소시킵니다. | Burgener, SS., et al. 2019. Cell Rep. 27: 3646-3656.e5. PMID: 31216481
- 메타카스파제 억제제의 스크리닝 및 동정: 억제 메커니즘 및 트리파노사이드 활성 평가. | Pérez, B., et al. 2021. Antimicrob Agents Chemother. 65: PMID: 33318019
- 가역적 광전환성 억제제는 평형을 벗어난 효소 반응에서 초민감성을 생성합니다. | Teders, M., et al. 2021. J Am Chem Soc. 143: 5709-5716. PMID: 33844531
- 급성 및 후기 대장염에서 생리활성 펩타이드 및 프로테아제 활성화 수용체의 단백질 분해 분해. | De Bruyn, M., et al. 2021. Int J Mol Sci. 22: PMID: 34639054
- 세린 프로테아제 억제제가 장 손상과 함께 다양한 설치류 모델에서 내장 통증에 미치는 영향. | Ceuleers, H., et al. 2022. Front Pharmacol. 13: 765744. PMID: 35721192
- 해양성 펠라기 곰팡이 균주의 세포 외 효소 활성과 온도의 영향. | Salazar Alekseyeva, K., et al. 2022. J Fungi (Basel). 8: PMID: 35736054
- 아형 선택적 사이클로필린 억제제의 발견 및 분자적 기초. | Peterson, AA., et al. 2022. Nat Chem Biol. 18: 1184-1195. PMID: 36163383
의 서브스트레이트:
Fluorogenic.주문정보
| 제품명 | 카탈로그 번호 | 단위 | 가격 | 수량 | 관심품목 | |
Chymotrypsin Substrate II, Fluorogenic, 25 mg | sc-391097 | 25 mg | $193.00 |
