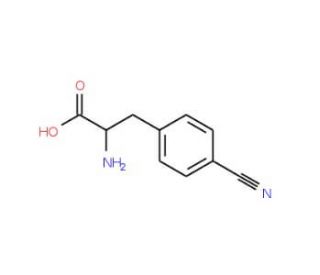
4-Cyano-L-phenylalanine (CAS 104531-20-6)
빠른 링크
4-시아노-L-페닐알라닌은 아미노산 유도체로 방향족 아미노산 계열에 속한다. 4-시아노-L-페닐알라닌은 페닐알라닌 분자에 결합된 시아노(CN) 그룹이 존재하는 것이 특징이다. 4-시아노-L-페닐알라닌은 과학 연구에서 독특한 화학적 특성으로 인해 다양한 용도로 사용된다. 펩티드 합성 및 약물 발견에서 빌딩 블록 또는 전구체로 일반적으로 사용된다. 시아노기는 다양한 화학적 변형을 도입하고 생물학적 활성이 변경된 펩티드 유사체를 생성하는 다용도 작용기 역할을 할 수 있다. 4-시아노-L-페닐알라닌의 주요 응용 분야 중 하나는 의학 화학 분야이다. 연구자들은 이 화합물을 이용하여 생체 활성, 안정성 또는 약동학적 특성이 향상된 신규 펩티드를 개발한다. 펩티드 서열에 4-시아노-L-페닐알라닌을 통합함으로써 과학자들은 펩티드가 수용체 또는 효소와 같은 생물학적 표적과 상호작용하는 것을 조절하여 잠재적으로 치료 효능을 향상시킬 수 있다. 4-시아노-L-페닐알라닌의 작용 메커니즘은 특정 맥락과 이것이 통합하는 펩티드 또는 분자에 따라 다르다. 4-시아노-L-페닐알라닌은 아미노산 유도체로서 합성되는 동안 펩티드 결합 형성에 참여하여 생성된 펩티드의 전체 구조 및 기능에 기여할 수 있다. 시아노기의 존재는 펩티드의 형태, 안정성 또는 수용체 결합 친화성을 변경함으로써 생물학적 표적과 펩티드의 상호작용에 영향을 미칠 수 있다. 나아가, 시아노기는 화학 반응을 통해 펩티드를 추가적으로 변형시키거나 기능화시킬 수 있다. 이러한 변형은 펩티드의 용해도, 막 투과성 또는 대사 안정성에 영향을 주어 생물학적 시스템에서의 거동에 영향을 미칠 수 있다.
4-Cyano-L-phenylalanine (CAS 104531-20-6) 참고자료
- 조합 화학 방법으로 선택된 P(1) 위치에 비천연 방향족 아미노산 잔기를 포함하는 인간 호중구 켑신 G의 새로운 발색 기질. | Wysocka, M., et al. 2007. Mol Divers. 11: 93-9. PMID: 17653609
- 단백질 환경의 진동 리포터로서 4-시아노-L-페닐알라닌의 유용성 확대. | Bazewicz, CG., et al. 2012. J Phys Chem B. 116: 10824-31. PMID: 22909326
- 아연 프탈로시아닌 결합 단백질의 합리적 설계. | Mutter, AC., et al. 2014. J Struct Biol. 185: 178-85. PMID: 23827257
- 국소 단백질 환경에 대한 민감하고 부위 특이적이며 안정적인 진동 프로브: 4-아지도메틸-L-페닐알라닌. | Bazewicz, CG., et al. 2013. J Phys Chem B. 117: 8987-93. PMID: 23865850
- Trp222의 '게이트 키퍼' 역할은 2-클로로-1-페닐에탄올에 대한 디케토환원효소의 양성자 선호도를 결정합니다. | Ma, H., et al. 2014. PLoS One. 9: e103792. PMID: 25072248
- 자도마이신 4-아미노-엘-페닐알라닌의 분리 및 합성 다각화. | Martinez-Farina, CF., et al. 2015. J Nat Prod. 78: 1208-14. PMID: 26035093
- 엔지니어링된 tRNA(Tyr) 억제제에 의한 비규범적 아미노산 통합 개선. | Rauch, BJ., et al. 2016. Biochemistry. 55: 618-28. PMID: 26694948
- 분광 리포터 비 천연 아미노산의 효과 조사: 구조적 연구. | Dippel, AB., et al. 2016. Acta Crystallogr D Struct Biol. 72: 121-30. PMID: 26894540
- 생물학적 발색단 비교: 시아노페닐알라닌 유도체의 광물리학적 특성. | Martin, JP., et al. 2016. Phys Chem Chem Phys. 18: 20750-7. PMID: 27412819
- 단백질 기능에 대한 최소한의 적외선 및 형광 프로브. | Gosavi, PM. and Korendovych, IV. 2016. Curr Opin Chem Biol. 34: 103-109. PMID: 27599185
- 분광 리포터 4-시아노-엘-페닐알라닌을 사용하여 헴 단백질의 국소 용해 환경을 탐색합니다. | Kearney, C., et al. 2018. RSC Adv. 8: 13503-13512. PMID: 29780583
- 천연 아미노산 4-니트로-L-페닐알라닌이 포함된 녹색 형광 단백질의 결정 구조. | Maurici, N., et al. 2018. Acta Crystallogr F Struct Biol Commun. 74: 650-655. PMID: 30279317
- 슈퍼폴더 녹색 형광 단백질에서 두 개의 비천연 아미노산 변색 발색단에 대한 구조적 및 분광광도학적 조사. | Olenginski, GM., et al. 2021. Acta Crystallogr D Struct Biol. 77: 1010-1018. PMID: 34342274
- 세포 전달 및 세포 내 국소화를 위해 새롭게 설계된 펩타이드. | Rhys, GG., et al. 2022. Nat Chem Biol. 18: 999-1004. PMID: 35836017
- 4-시아노-엘-페닐알라닌으로 복잡한 국소 단백질 환경의 해명. | Lee, B., et al. 2022. J Phys Chem B. 126: 8957-8969. PMID: 36317866
주문정보
| 제품명 | 카탈로그 번호 | 단위 | 가격 | 수량 | 관심품목 | |
4-Cyano-L-phenylalanine, 1 g | sc-290253 | 1 g | $156.00 | |||
4-Cyano-L-phenylalanine, 5 g | sc-290253A | 5 g | $604.00 |
