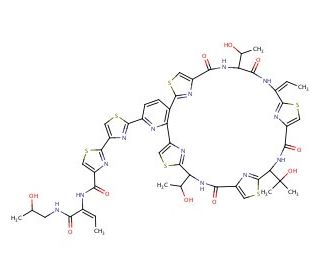
Thiocillin I (CAS 59979-01-0)
LINK RAPIDI
La tiocillina I, un antibiotico tiopeptidico, è riconosciuta principalmente per il suo ruolo nell'inibire la sintesi proteica batterica attraverso un meccanismo d'azione unico che ha come bersaglio il ribosoma. In particolare, si lega alla subunità ribosomiale 50S, interferendo con l'assemblaggio del centro di trasferimento dei peptidi, fondamentale per la traduzione delle proteine. Questa azione interrompe la sintesi di proteine essenziali necessarie per la crescita e la vitalità dei batteri, rendendo la tiocillina I uno strumento prezioso nella ricerca microbiologica volta a comprendere le complesse funzioni ribosomiali e l'azione degli antibiotici. Il suo utilizzo nella ricerca si estende allo studio dei meccanismi d'azione degli antibiotici tiopeptidici e del loro ruolo nella lotta alla resistenza agli antibiotici. La tiocillina I è particolarmente utile per sondare le basi genetiche della resistenza e della suscettibilità tra vari ceppi batterici, contribuendo a spiegare come i batteri si evolvono per resistere a tali potenti inibitori della sintesi proteica. Inoltre, questo composto contribuisce all'esplorazione di nuove strategie antibatteriche e alla potenziale modifica degli antibiotici esistenti per aumentarne l'efficacia contro i ceppi resistenti. La ricerca sulla tiocillina I continua a fornire importanti informazioni sulle complessità della sintesi proteica batterica e sullo sviluppo della resistenza, fondamentali per il progresso della microbiologia di base e della ricerca sugli antibiotici.
Thiocillin I (CAS 59979-01-0) Referenze
- Biosintesi dei tiopeptidi con peptidi precursori sintetizzati a livello ribosomiale e modifiche post-traslazionali conservate. | Liao, R., et al. 2009. Chem Biol. 16: 141-7. PMID: 19246004
- Attività inibitoria del proteasoma degli antibiotici tiazolici. | Pandit, B., et al. 2011. Cancer Biol Ther. 11: 43-7. PMID: 21119308
- Sintesi totale e assegnazione strutturale completa della tiocillina I. | Aulakh, VS. and Ciufolini, MA. 2011. J Am Chem Soc. 133: 5900-4. PMID: 21446660
- La mutagenesi in saturazione dell'Ala4 di TsrA svela un residuo altamente mutabile del tiostrepton A. | Zhang, F. and Kelly, WL. 2015. ACS Chem Biol. 10: 998-1009. PMID: 25572285
- La struttura di SpnF, un enzima autonomo che catalizza la cicloaddizione [4 + 2]. | Fage, CD., et al. 2015. Nat Chem Biol. 11: 256-8. PMID: 25730549
- Sintesi totale di micrococcina P1 e tiocillina I grazie al catalizzatore Mo(vi). | Akasapu, S., et al. 2019. Chem Sci. 10: 1971-1975. PMID: 30881626
- Lo screening virtuale identifica l'acido chebulagico come un inibitore del canale ionico virale M2(S31N) e del virus dell'influenza A. | Duncan, MC., et al. 2020. Molecules. 25: PMID: 32599753
- Forte sinergia tra la batteriocina tiopeptidica Micrococcin P1 e la rifampicina contro MRSA in un modello di infezione cutanea murina. | Ovchinnikov, KV., et al. 2021. Front Immunol. 12: 676534. PMID: 34276663
- Interazioni interspecie dinamiche e robustezza in un biofilm modello a quattro specie. | Baliarda, A., et al. 2021. Microbiologyopen. 10: e1254. PMID: 34964290
- Attivazione catalitica di ammidi con complessi di diossido di molibdeno(VI) termicamente stabili. | Evenson, GE., et al. 2023. J Org Chem. 88: 6192-6202. PMID: 37027833
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Thiocillin I, 500 µg | sc-391644 | 500 µg | $250.00 |
