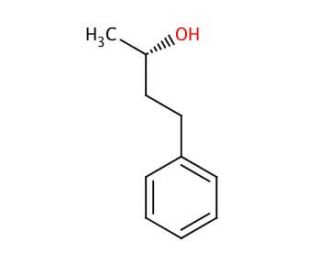

(S)-(+)-4-Phenyl-2-butanol (CAS 22148-86-3)
LINK RAPIDI
Il (S)-(+)-4-fenil-2-butanolo, un alcol secondario chirale, è un composto intrigante per i ricercatori a causa della sua specifica stereochimica. Questa molecola presenta una catena di quattro carboni con un gruppo fenile attaccato al quarto carbonio e un gruppo funzionale alcolico al secondo carbonio, il che la rende un prezioso intermedio nella sintesi di molecole organiche complesse. La sua configurazione (S)- è particolarmente degna di nota, in quanto svolge un ruolo cruciale nei processi di sintesi enantioselettiva, dove è richiesta la creazione di sostanze stereochimicamente pure. La presenza del gruppo fenile ne aumenta la reattività e lo rende un elemento cardine nella costruzione di composti aromatici. L'utilità di questo composto si estende a vari campi della ricerca chimica, tra cui la scienza dei materiali e la catalisi, dove la sua struttura unica può influenzare le proprietà e la reattività dei materiali sintetizzati. Il suo ruolo nello sviluppo di catalizzatori chirali, ligandi e altre strutture stereochimicamente complesse è di particolare interesse, a dimostrazione della sua versatilità e della sua importanza nell'avanzamento delle frontiere della ricerca chimica. Inoltre, il (S)-(+)-4-fenil-2-butanolo agisce come solvente nelle reazioni organiche. Studi sugli animali indicano il suo potenziale di riduzione dell'infiammazione e di alleviamento del dolore (effetti anti-nocicettivi). Inoltre, studi su colture cellulari rivelano le sue proprietà antiossidanti e antitumorali. Il (S)-(+)-4-fenil-2-butanolo inibisce anche la ciclossigenasi-2 (COX-2), un enzima coinvolto nella produzione di prostaglandine.
(S)-(+)-4-Phenyl-2-butanol (CAS 22148-86-3) Referenze
- Protezione dell'ambiente ed economia delle risorse mediante sintesi elettroorganiche ed elettroenzimatiche. | Steckhan, E., et al. 2001. Chemosphere. 43: 63-73. PMID: 11233827
- Complessi di rutenio aminociclopentadienile come catalizzatori di racemizzazione per la risoluzione cinetica dinamica di alcoli secondari a temperatura ambiente. | Choi, JH., et al. 2004. J Org Chem. 69: 1972-7. PMID: 15058942
- Riduzione e ossidazione asimmetrica di chetoni aromatici e alcoli utilizzando l'alcol deidrogenasi secondaria W110A di Thermoanaerobacter ethanolicus. | Musa, MM., et al. 2007. J Org Chem. 72: 30-4. PMID: 17194078
- Un derivato mutante dell'alcol deidrogenasi secondaria di Thermoanaerobacter ethanolicus altamente attivo e stereoselettivo su fenilacetone e benzilacetone. | Ziegelmann-Fjeld, KI., et al. 2007. Protein Eng Des Sel. 20: 47-55. PMID: 17283007
- L'alcol deidrogenasi secondaria W110A di Thermoanaerobacter ethanolicus, incapsulata in Xerogel, esegue la riduzione asimmetrica di chetoni idrofobici in solventi organici. | Musa, MM., et al. 2007. Angew Chem Int Ed Engl. 46: 3091-4. PMID: 17361973
- Derattizzazione di alcoli secondari mediante ossidazione e riduzione biocatalitica tandem. | Voss, CV., et al. 2008. Angew Chem Int Ed Engl. 47: 741-5. PMID: 18072189
- Recenti progressi nelle reazioni tandem asimmetriche promosse da multicatalizzatori. | Zhou, J. 2010. Chem Asian J. 5: 422-34. PMID: 20052703
- Acetofenone reduttasi con estrema stabilità rispetto a un'alta concentrazione di composti organici o a una temperatura elevata. | Yamamoto, T., et al. 2013. Appl Microbiol Biotechnol. 97: 10413-21. PMID: 23504059
- Racemizzazione di alcoli secondari enantiopuri da parte di Thermoanaerobacter ethanolicus secondary alcohol dehydrogenase. | Musa, MM., et al. 2013. Org Biomol Chem. 11: 2911-5. PMID: 23525226
- Un approccio di ricerca genomica per identificare le reduttasi carboniliche in Gluconobacter oxydans per la riduzione enantioselettiva dei chetoni. | Chen, R., et al. 2014. Biosci Biotechnol Biochem. 78: 1350-6. PMID: 25130736
- Pallavolo elettrocatalitica: Ciclo rapido di nicotinammide nanoconfinata per la sintesi organica nei pori dell'elettrodo. | Megarity, CF., et al. 2019. Angew Chem Int Ed Engl. 58: 4948-4952. PMID: 30633837
- Catalisi cooperativa di un'alcol deidrogenasi e di organosilice mesoporoso rodiato. | Himiyama, T., et al. 2019. Angew Chem Int Ed Engl. 58: 9150-9154. PMID: 31025503
- Derattizzazione e stereoinversione da parte di una cascata enzimatica bidirezionale nanoconfinata: doppio controllo tramite elettrochimica e attivazione selettiva di ioni metallici. | Cheng, B., et al. 2022. Chem Commun (Camb). 58: 11713-11716. PMID: 36178369
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
(S)-(+)-4-Phenyl-2-butanol, 1 g | sc-229224 | 1 g | $120.00 |
