OU749 (CAS 519170-13-9)
LINK RAPIDI
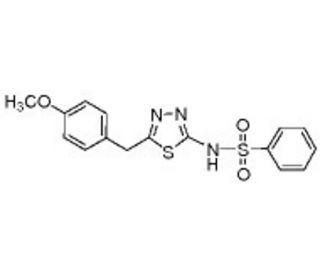
La N-[5-[(4-metossifenil)metil]-1,3,4-tidiazol-2-il]-benzensolfonammide, nota come OU749, si distingue nella ricerca per il suo ruolo di inibitore non competitivo della gamma-glutamil transpeptidasi (GGT), un enzima coinvolto nel metabolismo del glutatione e nel trasporto degli aminoacidi. Inibendo la GGT, OU749 viene utilizzato per studiare la funzione dell'enzima in questi processi biologici critici e la sua inibizione non competitiva suggerisce che si lega al complesso enzima-substrato, offrendo una prospettiva unica per esplorare la cinetica enzimatica della GGT e i potenziali meccanismi di regolazione. Le società tiadiazoliche e benzenesulfonamidiche del composto possono contribuire alla sua affinità e specificità di legame, rendendolo una sonda preziosa per chiarire i requisiti strutturali dell'inibizione della GGT. I ricercatori utilizzano OU749 per analizzare il ruolo dell'enzima nei processi cellulari, come la risposta allo stress ossidativo e le vie di disintossicazione, il che può portare a una comprensione più approfondita del coinvolgimento della GGT nei sistemi biologici e contribuire alla progettazione di nuovi inibitori con potenziali applicazioni di ricerca.
OU749 (CAS 519170-13-9) Referenze
- Una nuova classe, specie-specifica, di inibitori non competitivi della gamma-glutamil-transpeptidasi. | King, JB., et al. 2009. J Biol Chem. 284: 9059-65. PMID: 19203993
- Effetti divergenti dei composti sulle reazioni di idrolisi e transpeptidazione della γ-glutamil transpeptidasi. | Wickham, S., et al. 2012. J Enzyme Inhib Med Chem. 27: 476-89. PMID: 21864033
- Sperimentazione della specificità di substrato donatore e accettore della γ-glutamil transpeptidasi. | Hu, X., et al. 2012. Biochemistry. 51: 1199-212. PMID: 22257032
- Inibizione della γ-glutamil transpeptidasi umana: sviluppo di inibitori più potenti, fisiologicamente rilevanti e non competitivi. | Wickham, S., et al. 2013. Biochem J. 450: 547-57. PMID: 23301618
- Ruolo controverso dell'attività della gamma-glutamil transferasi nella nefrotossicità del cisplatino. | Fliedl, L., et al. 2014. ALTEX. 31: 269-78. PMID: 24664430
- La γ-Glutamil Transpeptidasi 1 umana: STRUTTURE DELL'ENZIMA LIBERO, DEGLI STATI DI TRANSIZIONE TETRAEDRIALI LEGATI ALL'INIBITORE E DELL'ENZIMA LEGATO AL GLUTAMATO RIVELANO UN NUOVO MOVIMENTO ALL'INTERNO DEL SITO ATTIVO DURANTE LA CATALISI. | Terzyan, SS., et al. 2015. J Biol Chem. 290: 17576-86. PMID: 26013825
- L'interazione tra cistina e glutatione è fondamentale per la regolazione delle vie di segnalazione degli aminoacidi e della ferroptosi. | Yu, X. and Long, YC. 2016. Sci Rep. 6: 30033. PMID: 27425006
- La gamma-glutamiltransferasi 1 promuove l'inizio e la progressione del carcinoma renale a cellule chiare. | Bansal, A., et al. 2019. Mol Cancer Res. 17: 1881-1892. PMID: 31151999
- L'alterazione dell'attività Mrp-1 like indotta dall'arsenico porta all'apoptosi degli epatociti di zebrafish: Il legame con il GSH cellulare. | Ray, A., et al. 2020. Environ Toxicol Pharmacol. 79: 103427. PMID: 32470611
- Una revisione sistematica della γ-Glutamiltransferasi sierica come biomarcatore prognostico nei pazienti con cancro genitourinario. | Takemura, K., et al. 2021. Antioxidants (Basel). 10: PMID: 33916150
- Lotta contro i tumori resistenti ai farmaci mediante l'inibizione della γ-glutamil transferasi con nano-assemblaggi supramolecolari di farmaci a base di platino. | Wang, L., et al. 2021. J Mater Chem B. 9: 4587-4595. PMID: 34059856
- L'espressione della gamma-glutamiltransferasi 1 nelle cellule di glioblastoma conferisce resistenza alla ferroptosi indotta dalla cistina. | Hayashima, K. and Katoh, H. 2022. J Biol Chem. 298: 101703. PMID: 35148992
- Progettazione e valutazione di nuovi analoghi dell'acido 2-amino-4-boronobutanoico (ABBA) come inibitori della gamma-glutamil-transpeptidasi umana. | Nguyen, L., et al. 2022. Bioorg Med Chem. 73: 116986. PMID: 36208545
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
OU749, 5 mg | sc-253219 | 5 mg | $132.00 |
