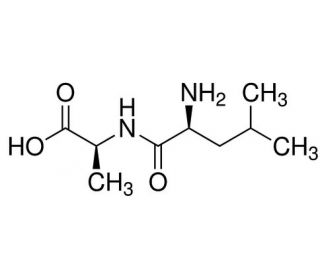
L-Leucyl-L-alanine (CAS 7298-84-2)
LINK RAPIDI
La L-Leucil-L-Alanina è un dipeptide che inibisce il degrado delle proteine mediato dall'ubiquitina. Viene utilizzata come intensificatore di fluorescenza nei metodi fluorimetrici per la determinazione della fenilalanina. La L-Leucil-L-Alanina è stata oggetto di studi in vitro per comprendere i suoi effetti sulle colture cellulari, in particolare il suo impatto sulla crescita e sulla differenziazione cellulare. Sebbene il meccanismo d'azione della L-Leucil-L-Alanina non sia completamente compreso, si ipotizza che funzioni come substrato per enzimi che svolgono un ruolo nella sintesi delle proteine e nel metabolismo dell'energia. Inoltre, si ritiene che sia coinvolta nella regolazione dell'espressione genica e nelle vie di segnalazione cellulare. Gli studiosi hanno scoperto che la L-Leucil-L-Alanina ha la capacità di stimolare la produzione di citochine, tra cui l'interleuchina-1β e il fattore di necrosi tumorale-α, che sono essenziali nella risposta immunitaria. Inoltre, ha dimostrato proprietà antimicrobiche contro varie bacteri come Escherichia coli, Staphylococcus aureus e Pseudomonas aeruginosa. Il composto è stato anche studiato per il suo potenziale come agente anti-infiammatorio.
L-Leucyl-L-alanine (CAS 7298-84-2) Referenze
- Stima della divergenza genetica e identificazione di tre specie di Trichinella mediante analisi isoenzimatica. | Snábel, V., et al. 2001. Parasite. 8: S30-3. PMID: 11484377
- Effetti della combinazione di un inibitore del proteasoma (PSI) e di un inibitore delle ubiquitine-ligasi (Leu-Ala) sull'ultrastruttura delle cellule leucemiche umane U937. | Biały, LP., et al. 2002. Folia Histochem Cytobiol. 40: 135-6. PMID: 12056612
- Espressione, purificazione e caratterizzazione di una proteina trasportatrice di riboflavina di pollo minimizzata da un gene sintetico in Escherichia coli. | Subramanian, S., et al. 2002. Protein Expr Purif. 26: 284-9. PMID: 12406683
- [Scissione rachimica di esteri di valil-glicina, leucil-glicina e alanil-beta-alanina]. | LOSSE, G., et al. 1959. Hoppe Seylers Z Physiol Chem. 314: 224-33. PMID: 13664211
- Lo sviluppo di coniugati VIP-ellittica. | Moody, TW., et al. 2004. Regul Pept. 123: 187-92. PMID: 15518911
- Progettazione, sintesi e struttura ai raggi X di potenti inibitori della memapsina 2 (beta-secretasi) con derivati isoftalamidici come leganti P2-P3. | Ghosh, AK., et al. 2007. J Med Chem. 50: 2399-407. PMID: 17432843
- Potenti inibitori della memapsina 2 (beta-secretasi): progettazione, sintesi, struttura ai raggi X della proteina-ligando e valutazione in vivo. | Ghosh, AK., et al. 2008. Bioorg Med Chem Lett. 18: 1031-6. PMID: 18180160
- Costruzione di dimeri concatamerici di recettori 7TM accoppiati covalentemente. | Terpager, M., et al. 2009. J Recept Signal Transduct Res. 29: 235-45. PMID: 19747085
- Metaboliti antimicrobici di una nuova actinomycete alofila, Nocardiopsis terrae YIM 90022. | Tian, S., et al. 2014. Nat Prod Res. 28: 344-6. PMID: 24236566
- Variazione genetica della peptidasi e della pirofosfatasi nel pollo. | Lundin, LG. and Wilhelmson, M. 1989. Poult Sci. 68: 1313-8. PMID: 2555801
- Potenti agonisti del recettore del complemento C3a derivati da aminoacidi ossazolici: relazioni struttura-attività. | Singh, R., et al. 2015. Bioorg Med Chem Lett. 25: 5604-8. PMID: 26522948
- Purificazione e identificazione di peptidi antinfiammatori derivati da digestati gastrointestinali simulati di proteine del corno di velluto (Cervus elaphus Linnaeus). | Zhao, L., et al. 2016. J Food Drug Anal. 24: 376-384. PMID: 28911592
- Siti di idrolisi dei dipeptidi in relazione ai siti di trasporto attivo dell'istidina e del glucosio nell'intestino del criceto. | Wiseman, G. 1983. J Physiol. 342: 421-35. PMID: 6631743
- Isolamento e delucidazione della struttura di due nuovi inibitori della calpaina da Streptomyces griseus. | Alvarez, ME., et al. 1994. J Antibiot (Tokyo). 47: 1195-201. PMID: 8002381
- Analisi dell'aminopeptidasi e della dipeptidilpeptidasi IV del fungo entomopatogeno Metarhizium anisopliae. | St Leger, RJ., et al. 1993. J Gen Microbiol. 139: 237-43. PMID: 8094738
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
L-Leucyl-L-alanine, 1 g | sc-300885 | 1 g | $92.00 | |||
L-Leucyl-L-alanine, 5 g | sc-300885A | 5 g | $240.00 | |||
L-Leucyl-L-alanine, 25 g | sc-300885B | 25 g | $999.00 | |||
L-Leucyl-L-alanine, 100 g | sc-300885C | 100 g | $3937.00 |
