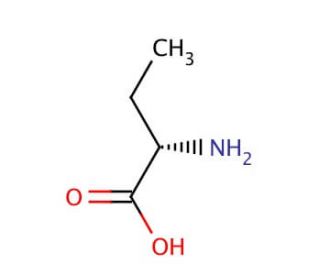
Struttura molecolare di L-Aminobutyric Acid, Numero CAS: 1492-24-6
L-Aminobutyric Acid (CAS 1492-24-6)
Nomi alternativi:
L(+)-2-Aminobutyric acid; H-Abu-OH
Applicazione:
L-Aminobutyric Acid è un antagonista dei recettori
Numero CAS:
1492-24-6
Purezza:
≥98%
Peso molecolare:
103.12
Formula molecolare:
C4H9NO2
Solo per uso in Ricerca. Non previsto per Uso Diagnostico o Terapeutico.
* Vedere Certificato di Analisi per informazioni sul lotto specifico (incluso il contenuto d'acqua).
LINK RAPIDI
Informazioni ordini
Descrizione
Informazione tecnica
Informazioni di sicurezza
SDS & Certificato d'analisi
L'acido L-aminobutirrico è un aminoacido non proteico. È un importante neurotrasmettitore inibitorio del sistema nervoso centrale, dove regola l'eccitabilità neuronale. L'acido L-aminobutirrico è coinvolto nella modulazione del tono muscolare e svolge un ruolo nella regolazione dell'ansia e dello stress. Viene sintetizzato dal glutammato dall'enzima glutammato decarbossilasi ed è immagazzinato nelle vescicole sinaptiche. Al momento del rilascio, l'acido L-aminobutirrico si lega a specifici recettori sulla membrana postsinaptica, determinando l'apertura dei canali dei cloruri e l'iperpolarizzazione del neurone. Ciò determina l'inibizione dell'accensione dei neuroni e della trasmissione degli impulsi nervosi.
L-Aminobutyric Acid (CAS 1492-24-6) Referenze
- Distribuzione dell'immunoreattività della glicina nel cervello dello storione siberiano (Acipenser baeri): confronto con l'acido γ-aminobutirrico. | Adrio, F., et al. 2011. J Comp Neurol. 519: 1115-42. PMID: 21344405
- Risoluzione cinetica dinamica enzimatica di N-formil- e N-carbamoil-amminoacidi racemici utilizzando L-N-carbamoilasi e N-succinil-amminoacido racemasi immobilizzate. | Soriano-Maldonado, P., et al. 2015. Appl Microbiol Biotechnol. 99: 283-91. PMID: 24993356
- Idratazione e rete di legami a idrogeno dell'acqua intorno a una superficie idrofobica studiata con la spettroscopia terahertz. | Shiraga, K., et al. 2014. J Chem Phys. 141: 235103. PMID: 25527962
- Correlazione sperimentale della posizione del substrato con l'esito della reazione nell'alogenasi alifatica SyrB2. | Martinie, RJ., et al. 2015. J Am Chem Soc. 137: 6912-9. PMID: 25965587
- Sintesi e proprietà dei -cianoaminoacidi. -Cianoglicina, L-ciano-alanina e acido L-aminobutirrico. | Ressler, C., et al. 1971. J Org Chem. 36: 3960-6. PMID: 5127992
- Eliminazione enzimatica del fluoro dall'alfa-fluoro-beta-alanina. | Porter, DJ., et al. 1995. Biochem Pharmacol. 50: 1475-84. PMID: 7503799
- Purificazione di peptide sintetasi coinvolte nella biosintesi della pristinamicina I. | Thibaut, D., et al. 1997. J Bacteriol. 179: 697-704. PMID: 9006023
- Biosintesi di pristinamicina I in Streptomyces pristinaespiralis: caratterizzazione molecolare dei primi due geni della peptide sintetasi strutturale. | de Crécy-Lagard, V., et al. 1997. J Bacteriol. 179: 705-13. PMID: 9006024
- Utilizzo degli aminoacidi da parte del fitoplancton marino: un nuovo meccanismo | Palenik, B., & Morel, F. M. 1990. Limnology and Oceanography. 35(2): 260-269.
- Specificità della lisina: N6-idrossilasi: un'ipotesi per un substrato intermedio reattivo nel meccanismo catalitico | Marrone, L., Siemann, S., Beecroft, M., & Viswanatha, T. 1996. Bioorganic Chemistry. 24(4): 401-416.
- Studi sull'interazione tra α-amminoacidi con catene laterali polari e composti eterociclici a T= 298,15 K. | Yu, L., Hu, X. G., Lin, R. S., & Xu, G. Y. 2004. The Journal of Chemical Thermodynamics. 36(6): 483-490.
- Studi sulle interazioni tra alcuni α-amminoacidi con catena laterale non polare e due eteri ciclici saturi a 298,15 K: misurazione entalpica e simulazione al computer | Yu, L., Yuan, S. L., Hu, X. G., & Lin, R. S. 2006. Chemical engineering science. 61(2): 794-801.
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
L-Aminobutyric Acid, 5 g | sc-218628 | 5 g | $62.00 |
