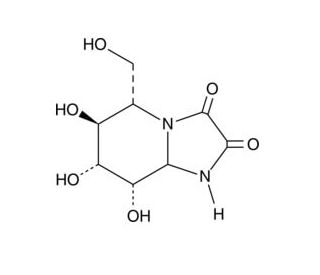
Kifunensine (CAS 109944-15-2)
See product citations (25)
QUICK LINKS
Kifunensine is a chemical compound that is particularly valuable in the field of glycobiology research. It acts as a potent inhibitor of mannosidase I, an enzyme involved in the modification of glycoproteins during their maturation in the endoplasmic reticulum. By interfering with this enzyme, kifunensine is used to study the folding and quality control of glycoproteins, as well as their trafficking through the secretory pathway. Its inhibition of mannosidase I results in the production of glycoproteins with a high-mannose glycan profile, which is useful for examining protein folding disorders and for enhancing the stability and efficacy of certain glycoproteins. Additionally, kifunensine has applications in the development of biologics, where controlling glycosylation patterns is for the activity and half-life of chemicals. It also finds utility in the synthesis of homogeneous glycoproteins for structural and functional analyses.
Kifunensine (CAS 109944-15-2) References
- A practical synthesis of kifunensine analogues as inhibitors of endoplasmic reticulum alpha-mannosidase I. | Hering, KW., et al. 2005. J Org Chem. 70: 9892-904. PMID: 16292820
- Glycosidase inhibitors: inhibitors of N-linked oligosaccharide processing. | Elbein, AD. 1991. FASEB J. 5: 3055-63. PMID: 1743438
- Kifunensine inhibits glycoprotein processing and the function of the modified LDL receptor in endothelial cells. | Elbein, AD., et al. 1991. Arch Biochem Biophys. 288: 177-84. PMID: 1898016
- Kifunensine, a potent inhibitor of the glycoprotein processing mannosidase I. | Elbein, AD., et al. 1990. J Biol Chem. 265: 15599-605. PMID: 2144287
- Synthesis of kifunensine thioanalogs and their inhibitory activities against HIV-RT and α-mannosidase. | Chen, H., et al. 2013. Carbohydr Res. 365: 1-8. PMID: 23159373
- Conformational Analysis of the Mannosidase Inhibitor Kifunensine: A Quantum Mechanical and Structural Approach. | Males, A., et al. 2017. Chembiochem. 18: 1496-1501. PMID: 28493500
- Glycoform Modification of Secreted Recombinant Glycoproteins through Kifunensine Addition during Transient Vacuum Agroinfiltration. | Xiong, Y., et al. 2018. Int J Mol Sci. 19: PMID: 29562594
- In Vivo Glycan Engineering via the Mannosidase I Inhibitor (Kifunensine) Improves Efficacy of Rituximab Manufactured in Nicotiana benthamiana Plants. | Kommineni, V., et al. 2019. Int J Mol Sci. 20: PMID: 30621113
- Pharmacologic inhibition of N-linked glycan trimming with kifunensine disrupts GLUT1 trafficking and glucose uptake. | Lodge, EK., et al. 2020. Biochimie. 174: 18-29. PMID: 32298759
- A class of low-cost alternatives to kifunensine for increasing high mannose N-linked glycosylation for monoclonal antibody production in Chinese hamster ovary cells. | Brantley, TJ., et al. 2021. Biotechnol Prog. 37: e3076. PMID: 32888259
- Effects of Kifunensine on Production and N-Glycosylation Modification of Butyrylcholinesterase in a Transgenic Rice Cell Culture Bioreactor. | Macharoen, K., et al. 2020. Int J Mol Sci. 21: PMID: 32962231
- Inhibition of SARS-CoV-2 viral entry upon blocking N- and O-glycan elaboration. | Yang, Q., et al. 2020. Elife. 9: PMID: 33103998
- Brefeldin A and kifunensine modulate LPS-induced lung endothelial hyperpermeability in human and bovine cells. | Kubra, KT. and Barabutis, N. 2021. Am J Physiol Cell Physiol. 321: C214-C220. PMID: 34161151
- A new immunomodulator, FR-900494: taxonomy, fermentation, isolation, and physico-chemical and biological characteristics. | Iwami, M., et al. 1987. J Antibiot (Tokyo). 40: 612-22. PMID: 3610820
- Disrupting N-Glycosylation Using Type I Mannosidase Inhibitors Alters B-Cell Receptor Signaling. | Huang, A., et al. 2022. ACS Pharmacol Transl Sci. 5: 1062-1069. PMID: 36407961
Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
Kifunensine, 1 mg | sc-201364 | 1 mg | $135.00 | |||
Kifunensine, 5 mg | sc-201364A | 5 mg | $540.00 | |||
Kifunensine, 10 mg | sc-201364B | 10 mg | $1025.00 | |||
Kifunensine, 100 mg | sc-201364C | 100 mg | $6248.00 |
