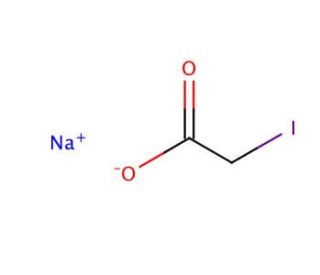
Iodoacetic acid sodium salt (CAS 305-53-3)
LINK RAPIDI
L'acido iodoacetico sale sodico, noto anche come iodoacetato di sodio, è un composto chimico ampiamente utilizzato in biochimica e nella ricerca di laboratorio per la sua capacità di modificare i residui di cisteina nelle proteine e di inibire le proteasi cisteiniche. Questo composto dimostra un effetto inibitorio minore su specifiche attività enzimatiche nel plasma di gallina. Si caratterizza per la sua solubilità in acqua e alcool, presentandosi come un solido bianco. Il suo ruolo si estende a diverse applicazioni di ricerca, come lo studio degli enzimi, l'analisi della struttura e del metabolismo delle proteine e l'esplorazione dei processi cellulari, tra cui la segnalazione cellulare e la funzionalità dei canali del sodio. La capacità dell'acido iodoacetico sale sodico di legarsi ai siti attivi degli enzimi, ostacolandone le funzioni catalitiche, lo rende uno strumento prezioso per la comprensione dei meccanismi proteici e cellulari, della sintesi di DNA e RNA e dell'espressione genica.
Iodoacetic acid sodium salt (CAS 305-53-3) Referenze
- Riformulazione in vitro dell'insulina: caratterizzazione degli intermedi e del percorso putativo di ripiegamento. | Tang, Y., et al. 2007. Sci China C Life Sci. 50: 717-25. PMID: 17914645
- Utilizzo preferenziale del NADPH come donatore endogeno di elettroni per la NAD(P)H:chinone ossidoreduttasi 1 (NQO1) in cellule endoteliali arteriose polmonari intatte. | Bongard, RD., et al. 2009. Free Radic Biol Med. 46: 25-32. PMID: 18848878
- Sintesi e valutazione di un nuovo analogo fotoreattivo dell'alfa-amminoacido con funzioni acide e clivabili. | Bongo, NB., et al. 2009. Bioorg Med Chem Lett. 19: 80-2. PMID: 19026535
- Sviluppo di una tecnica di plastinazione in fogli ultrasottili in articolazioni omerali di ratto con osteoartrite indotta da iodoacetato monosodico per lo studio della neovascolarizzazione. | Vargas, CA., et al. 2020. Anat Sci Int. 95: 297-303. PMID: 31401788
- Proprietà fisico-chimiche degli isomeri di carica della superossido dismutasi umana ricombinante. | Kajihara, J., et al. 1988. J Biochem. 104: 638-42. PMID: 3241003
- Riduzione e riossidazione della neurotossina II dello scorpione Androctonus australis Hector. | Sabatier, JM., et al. 1987. Int J Pept Protein Res. 30: 125-34. PMID: 3667073
- Interazione tra l'enzima tripsina-simile di Streptomyces erythraeus e l'ovomucoide di pollo. | Nagata, K. and Yoshida, N. 1984. J Biochem. 96: 1041-9. PMID: 6394596
- Metodo di idrolisi singolo per tutti gli aminoacidi, compresi cisteina e triptofano. | Inglis, AS. 1983. Methods Enzymol. 91: 26-36. PMID: 6855579
- Rilevazione simultanea di due meccanismi di distruzione immunitaria dei globuli rossi umani trattati con penicillina. | Yust, I., et al. 1982. Am J Hematol. 13: 53-62. PMID: 7137166
- Effetto di alcuni cationi metallici e composti organici sull'attività di idrolizzazione dell'O-esil O-2,5-diclorofenil fosforamidato nel plasma di gallina. | Sogorb, MA., et al. 1993. Arch Toxicol. 67: 416-21. PMID: 8215911
- Inibitori metabolici e ricongiungimento cromosomico | AV Beatty, JW Beatty - American Journal of Botany, 1959 - Wiley Online Library. May 1959. American Journal of Botany. Volume46, Issue5: Pages 317-323.
- Ripiegamento all'equilibrio del precursore dell'insulina suina in presenza di un tampone redox: Implicazioni per gli intermedi comuni condivisi dai suoi processi di unfolding/refolding | , et al. 2008,. Protein and Peptide Letters,. Volume 15, Number 9,: pp. 972-979(8).
- Caratterizzazione di una ficoeritrina intatta e della sua subunità funzionale scissa di 14 kDa dal cianobatterio marino Phormidium sp. A27DM | A Parmar, NK Singh, A Kaushal, D Madamwar - Process Biochemistry, 2011 - Elsevier. September 2011,. Process Biochemistry. Volume 46, Issue 9,: Pages 1793-1799.
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Iodoacetic acid sodium salt, 25 g | sc-204014 | 25 g | $125.00 |
