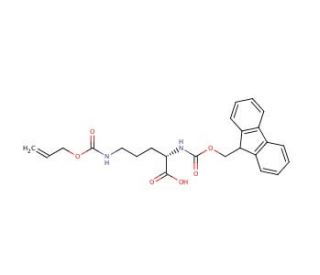
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7)
LINK RAPIDI
Fmoc-Orn(Alloc)-OH rappresenta un derivato dell'aminoacido Ornitina, presente in natura e che partecipa al metabolismo dell'azoto come intermedio nel ciclo dell'urea. Ampiamente impiegato nella sintesi organica e nella biochimica, questo derivato aminoacidico possiede una notevole versatilità. Ha molteplici scopi, tra cui la sintesi di proteine e peptidi, oltre a servire come materiale di partenza per la sintesi di vari composti. Nella ricerca scientifica, Fmoc-Orn(Alloc)-OH trova ampie applicazioni, in particolare nella sintesi di peptidi e proteine. La sua utilità risiede nell'introduzione di diversi gruppi funzionali in peptidi e proteine. Inoltre, questo composto viene utilizzato per sintetizzare altri composti come piccole molecole e polimeri. La sua capacità di introdurre un'ampia gamma di gruppi funzionali in questi composti è molto vantaggiosa. Il meccanismo d'azione di Fmoc-Orn(Alloc)-OH si basa sulla sua reattività con gli amminoacidi e altre molecole. Grazie alla sua interazione con un amminoacido, forma un legame covalente noto come legame peptidico, facilitando il collegamento degli amminoacidi per creare peptidi e proteine. Inoltre, Fmoc-Orn(Alloc)-OH può stabilire legami covalenti con piccole molecole e polimeri attraverso le sue reazioni con essi.
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7) Referenze
- Sintesi e generazione di anticorpi specifici per glicopeptidi con N-GlcNAcilazione di arginina. | Pan, M., et al. 2014. Angew Chem Int Ed Engl. 53: 14517-21. PMID: 25353391
- Rilevamento specifico in spettrometria di massa tandem dei residui di arginina modificati dagli AGE nei peptidi. | Schmidt, R., et al. 2015. J Mass Spectrom. 50: 613-24. PMID: 25800199
- Rilevamento selettivo del pirofosfato in mezzi fisiologici mediante peptidi dipicolilammino-funzionalizzati con zinco(II). | Zwicker, VE., et al. 2015. Org Biomol Chem. 13: 7822-9. PMID: 26107804
- Peptidi sintetici che mimano il sito di legame dell'acetilcolinesterasi umana per il suo inibitore fascicolina 2. | Kafurke, U., et al. 2015. J Pept Sci. 21: 723-30. PMID: 26200472
- La risoluzione del legame α-glicosidico del fattore P di allungamento della traduzione arginina-ramnosilato innesca la generazione del primo anticorpo specifico per ArgRha. | Li, X., et al. 2016. Chem Sci. 7: 6995-7001. PMID: 28451135
- Riconoscimento di analoghi della dimetilarginina da parte della proteina Spindlin1 con dominio tandem Tudor. | Porzberg, MRB., et al. 2022. Molecules. 27: PMID: 35164245
- Generazione biocompatibile e selettiva di peptidi biciclici. | Ullrich, S., et al. 2022. Angew Chem Int Ed Engl. 61: e202208400. PMID: 35852030
- Peptidi pegilati. II. Sintesi in fase solida di peptidi pegilati amminici, carbossilici e a catena laterale. | Lu, YA. and Felix, AM. 1994. Int J Pept Protein Res. 43: 127-38. PMID: 8200730
- Il duplice ruolo dell'acido fenilboronico come recettore per i carboidrati e come quencher per il fluoroforo pirene vicino | Lok Nath Neupane, Chuda Raj Lohani, Jeongho Kim, Keun-Hyeung Lee. 2013. Tetrahedron. 69: 11057-11063.
- Sintesi totale del dominio di morte TRADD con N-GlcNAcilazione dell'arginina mediante legatura chimica nativa a base di idrazide | Ye Wu a b 1, Yulei Li c 1, Wei Cong a, Yan Zou b, Xiang Li b, Honggang Hu a. 2020. Chinese Chemical Letters. 31: 107-110.
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Fmoc-Orn(Alloc)-OH, 5 g | sc-235198 | 5 g | $156.00 |
