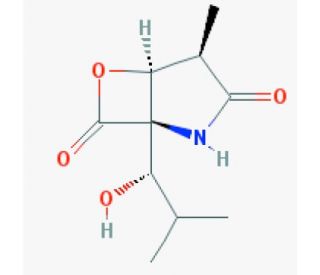
clasto-Lactacystin β-lactone (CAS 155975-72-7)
Vedere citazioni di prodotto (1)
LINK RAPIDI
Il clasto-lattacistina β-lattone (CAS: 155975-72-7) è una sostanza chimica di notevole interesse soprattutto per il suo ruolo di precursore della lattacistina, una molecola interessante nella ricerca biochimica per la sua capacità di modulare l'attività del proteasoma. Il clasto-lattacistina β-lattone stesso, quando viene metabolizzato, si trasforma in lattacistina, che successivamente interagisce con il proteasoma, un complesso proteico responsabile della degradazione delle proteine indesiderate o mal ripiegate nelle cellule. L'azione specifica del β-lattone della clasto-lattacistina comporta la sua conversione in diidrossiacido di clasto-lattacistina in presenza di nucleofili cellulari, che inibiscono l'attività proteasomica, mirando specificamente alle β-subunità proteolitiche all'interno del nucleo 20S del proteasoma. Questa inibizione è fondamentale per studiare i meccanismi di degradazione delle proteine in varie condizioni fisiologiche, fornendo così approfondimenti sulla regolazione del turnover proteico e sulle sue implicazioni nelle funzioni cellulari. I ricercatori utilizzano la clasto-lattacistina β-lattone per esplorare le dinamiche dell'inibizione del proteasoma e il suo impatto sull'omeostasi proteica all'interno delle cellule.
clasto-Lactacystin β-lactone (CAS 155975-72-7) Referenze
- Crescita dei neuriti nelle cellule PC12. Distinzione dei ruoli dell'ubiquitilazione e della proteolisi ubiquitina-dipendente. | Obin, M., et al. 1999. J Biol Chem. 274: 11789-95. PMID: 10206996
- Una nuova via sintetica enantioselettiva per ottenere analoghi dell'omuralide con un potenziale di selettività di specie nell'inibizione del proteasoma. | Crane, SN. and Corey, EJ. 2001. Org Lett. 3: 1395-7. PMID: 11348243
- Inibitori del proteasoma: da strumenti di ricerca a candidati farmaci. | Kisselev, AF. and Goldberg, AL. 2001. Chem Biol. 8: 739-58. PMID: 11514224
- Semplici sintesi enantiospecifiche dei diastereomeri C(2) dell'omuralide e del 3-metilomuralide. | Reddy, LR., et al. 2005. Org Lett. 7: 2703-5. PMID: 15957926
- Inibizione del proteasoma da parte di un beta-lattame totalmente sintetico correlato alla salinosporamide A e all'omuralide. | Hogan, PC. and Corey, EJ. 2005. J Am Chem Soc. 127: 15386-7. PMID: 16262399
- Previsione del meccanismo d'azione dell'omuralide (clasto-lattacistina beta-lattone) sulla catepsina A umana basata su un modello strutturale del complesso proteasoma beta5/PRE2-subunità di lievito/omuralide. | Aikawa, S., et al. 2006. Biochim Biophys Acta. 1764: 1372-80. PMID: 16870514
- Nuovo ingresso di isocianidi convertibili per la reazione di Ugi e sua applicazione alla sintesi totale formale stereocontrollata dell'inibitore del proteasoma omuralide. | Gilley, CB., et al. 2007. Org Lett. 9: 3631-4. PMID: 17672474
- Sintesi totali stereospecifiche degli inibitori del proteasoma omuralide e lattacistina. | Gu, W. and Silverman, RB. 2011. J Org Chem. 76: 8287-93. PMID: 21916437
- Omuralide e vibralattone: le differenze nell'impalcatura di legame proteasoma-β-lattone-γ-lattame alterano le preferenze del bersaglio. | List, A., et al. 2014. Angew Chem Int Ed Engl. 53: 571-4. PMID: 24285701
- Accesso stereocontrollato a δ-lattoni-γ-lattami fusi con stereocentri benzilici quaternari angolari. | Beng, TK., et al. 2022. RSC Adv. 12: 17617-17620. PMID: 35765420
- Inibizione delle attività del proteasoma e della modificazione amino-terminale-treonina specifica della subunità da parte della lattacistina. | Fenteany, G., et al. 1995. Science. 268: 726-31. PMID: 7732382
- Studi meccanici sull'inattivazione del proteasoma da parte della lattacistina in cellule coltivate. | Dick, LR., et al. 1997. J Biol Chem. 272: 182-8. PMID: 8995245
- Sintesi totale e attività biologica di lattacistina, omuralide e analoghi. | Corey, EJ. and Li, WD. 1999. Chem Pharm Bull (Tokyo). 47: 1-10. PMID: 9987821
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
clasto-Lactacystin β-lactone, 100 µg | sc-202106 | 100 µg | $254.00 |
