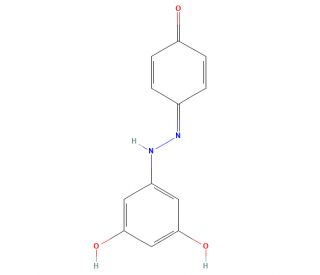
Azo-Resveratrol (CAS 1393556-48-3)
LINK RAPIDI
L'azorisveratrolo, un composto chimico versatile, trova ampio impiego in diverse applicazioni di ricerca scientifica. Come diolo, presenta due gruppi ossidrilici attaccati a un singolo atomo di carbonio, il che lo rende un composto di grande interesse per le sue proprietà distintive e il suo potenziale in diversi campi. Serve come componente chiave nella sintesi di polimeri, coloranti e altri materiali. Inoltre, svolge un ruolo significativo nello sviluppo di prodotti farmaceutici, tra cui agenti antitumorali e antinfiammatori. La sua utilità si estende allo studio della struttura e della funzione delle proteine e alla ricerca di inibitori enzimatici. Sebbene l'esatto meccanismo d'azione dell'azorisveratrolo sia ancora incompleto, si ipotizza che il composto agisca come inibitore di enzimi specifici, come la ciclossigenasi e la lipossigenasi. Inoltre, si ritiene che possieda proprietà antiossidanti, potenzialmente in grado di salvaguardare le cellule dai danni indotti dai radicali liberi.
Azo-Resveratrol (CAS 1393556-48-3) Referenze
- Sintesi di nuovi azo-resveratrolo, azo-ossirisveratrolo e loro derivati come potenti inibitori della tirosinasi. | Song, YM., et al. 2012. Bioorg Med Chem Lett. 22: 7451-5. PMID: 23142612
- Un nuovo inibitore della tirosinasi sintetizzato: (E)-2-((2,4-diidrossifenil)diazenil)fenil 4-metilbenzenesolfonato come analogo dell'azo-resveratrolo. | Bae, SJ., et al. 2013. Biosci Biotechnol Biochem. 77: 65-72. PMID: 23291747
- Valutazione dell'affinità di crocina e curcumina sulla tirosinasi dei funghi mediante risonanza plasmonica di superficie. | Patil, S., et al. 2014. Int J Biol Macromol. 65: 163-6. PMID: 24444880
- Progettazione e scoperta di inibitori della tirosinasi dei funghi e loro applicazioni terapeutiche. | Mendes, E., et al. 2014. Expert Opin Drug Discov. 9: 533-54. PMID: 24708040
- Inibitori naturali, semisintetici e sintetici della tirosinasi. | Lee, SY., et al. 2016. J Enzyme Inhib Med Chem. 31: 1-13. PMID: 25683082
- Agenti sbiancanti della pelle: prospettiva di chimica medicinale degli inibitori della tirosinasi. | Pillaiyar, T., et al. 2017. J Enzyme Inhib Med Chem. 32: 403-425. PMID: 28097901
- Controllo ottico reversibile della F1 Fo -ATP sintasi mediante inibitori fotoswitchabili. | Eisel, B., et al. 2018. FEBS Lett. 592: 343-355. PMID: 29292505
- Una rassegna completa sugli inibitori della tirosinasi. | Zolghadri, S., et al. 2019. J Enzyme Inhib Med Chem. 34: 279-309. PMID: 30734608
- Determinazione del resveratrolo e dei suoi derivati come neuroprotettori contro l'alterazione indotta da monocrotofos in proteine NIPBL e POU4F1 attraverso studi di docking molecolare. | Yadav, R. and Srivastava, P. 2020. Environ Sci Pollut Res Int. 27: 291-304. PMID: 31786755
- Progettazione, sintesi e valutazione biologica di derivati simmetrici dell'azina come nuovi inibitori della tirosinasi. | Karimian, S., et al. 2021. BMC Chem. 15: 54. PMID: 34587988
- Una classificazione organica aggiornata degli inibitori della tirosinasi sulla biosintesi della melanina. | Chen, C. Y., Lin, L. C., Yang, W. F., Bordon, J., & D Wang, H. M. (2015). Current Organic Chemistry,. 19(1):, 4-18.
- Vie sintetiche di derivati azoici: una breve panoramica. | Shah, H. U. R., Ahmad, K., Naseem, H. A., Parveen, S., Ashfaq, M., Aziz, T.,.. & Shahzad, A. (2021. Journal of Molecular Structure,. 1244,: 131181.
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Azo-Resveratrol, 10 mg | sc-503240 | 10 mg | $359.00 |
