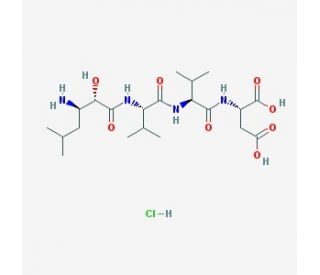
Amastatin hydrochloride (CAS 100938-10-1)
Vedere citazioni di prodotto (3)
LINK RAPIDI
L'amastatina cloridrato è un inibitore competitivo lento e strettamente legato dell'aminopeptidasi A del siero umano, dell'aminopeptidasi M del siero umano (CD13), della leucina aminopeptidasi del rene di maiale (LAP3) e dell'aminopeptidasi tirosinica, ma non dell'aminopeptidasi B. Il composto è stato utilizzato per potenziare l'azione di alcuni peptidi bioattivi inibendone la degradazione da parte delle aminopeptidasi. È stato dimostrato che l'amastatina cloridrato diminuisce leggermente la conversione dell'angiontensina II in angiotensina III, ma aumenta significativamente la potenza dell'angiotensina III e della des(Asp1)angiotensina I. Inoltre, le attività enzimatiche amidolitiche Suc-Ala-Ala-Pro-Leu-pNA sono state completamente inibite con l'aggiunta di amastatina cloridrato.
Amastatin hydrochloride (CAS 100938-10-1) Referenze
- Inibitori dell'attività di un enzima simile all'elastasi che catalizza l'amidolisi di Suc-Ala-Ala-Pro-Leu-pNA nel plasma seminale umano. | Matsuda, Y., et al. 2000. Arch Androl. 44: 1-9. PMID: 10690759
- Localizzazione dell'enzima carbossipeptidasi A-like nel rene di ratto. | Igić, R., et al. 2003. Peptides. 24: 1237-40. PMID: 14612196
- Purificazione e caratterizzazione dell'aminopeptidasi N di Spodoptera litura espressa in cellule di insetto Sf21. | Kaur, R., et al. 2007. Protein Expr Purif. 54: 267-74. PMID: 17467291
- Ruolo dell'attività delle aminopeptidasi nella regolazione dell'attività pressoria delle angiotensine circolanti. | Ahmad, S. and Ward, PE. 1990. J Pharmacol Exp Ther. 252: 643-50. PMID: 1968973
- Gli acidi biliari innescano il rilascio di GLP-1 prevalentemente attraverso l'accesso ai recettori degli acidi biliari accoppiati a proteine G situati in posizione basale. | Brighton, CA., et al. 2015. Endocrinology. 156: 3961-70. PMID: 26280129
- Un approccio in silico per comprendere le proprietà struttura-funzione di una serina proteasi (Bacifrinasi) di Bacillus cereus e prove sperimentali a sostegno dell'interazione della Bacifrinasi con fibrinogeno e trombina. | Bora, B., et al. 2017. J Biomol Struct Dyn. 35: 622-644. PMID: 26919276
- Secrezione di GLP-1 e PYY dipendente dal recettore di tipo 1 dell'angiotensina II nei topi e nell'uomo. | Pais, R., et al. 2016. Endocrinology. 157: 3821-3831. PMID: 27447725
- L'attività di Sirt1 nelle PBMC come biomarcatore di diversi fenotipi di insufficienza cardiaca. | Conti, V., et al. 2020. Biomolecules. 10: PMID: 33238655
- Il livello di attività del recettore ACE2 del SARS-CoV-2 è altamente elevato nei pazienti di età avanzata con stenosi aortica: implicazioni per l'ACE2 come biomarcatore della gravità della COVID-19. | Fagyas, M., et al. 2021. Geroscience. 43: 19-29. PMID: 33469835
- Consegna nasale di Atenololo e Timololo nel ratto ed effetto dei potenziatori dell'assorbimento. | Thadikonda, KP., et al. 1995. Drug Dev Ind Pharm. 21: 349-360. PMID: 36600544
- Inibizione delle aminopeptidasi da parte di amastatina e derivati della bestatina. Effetto della struttura dell'inibitore sui processi di legame lento. | Rich, DH., et al. 1984. J Med Chem. 27: 417-22. PMID: 6142952
- Amastatina, un inibitore dell'aminopeptidasi A, prodotto da actinomiceti. | Aoyagi, T., et al. 1978. J Antibiot (Tokyo). 31: 636-8. PMID: 681249
- Determinazione cristallografica a raggi X della struttura della leucina aminopeptidasi del cristallino bovino complessata con amastatina: formulazione di un meccanismo catalitico caratterizzato da uno stato di transizione gemma-diolato. | Kim, H. and Lipscomb, WN. 1993. Biochemistry. 32: 8465-78. PMID: 8357796
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
Amastatin hydrochloride, 1 mg | sc-202051 | 1 mg | $73.00 | |||
Amastatin hydrochloride, 5 mg | sc-202051A | 5 mg | $218.00 |
