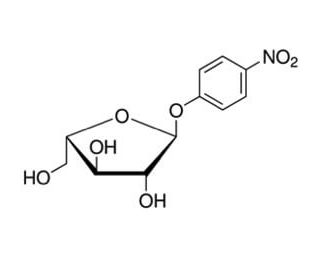
Struttura molecolare di 4-Nitrophenyl α-L-arabinofuranoside, Numero CAS: 6892-58-6
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6)
Vedere citazioni di prodotto (1)
Nomi alternativi:
pNP-alpha-L-Arabinofuranoside
Numero CAS:
6892-58-6
Purezza:
≥98%
Peso molecolare:
271.22
Formula molecolare:
C11H13NO7
Solo per uso in Ricerca. Non previsto per Uso Diagnostico o Terapeutico.
* Vedere Certificato di Analisi per informazioni sul lotto specifico (incluso il contenuto d'acqua).
LINK RAPIDI
Informazioni ordini
Citazioni prodotti
Descrizione
Informazione tecnica
Informazioni di sicurezza
SDS & Certificato d'analisi
Il 4-Nitrofenil α-L-arabinofuranoside è un composto sintetico spesso utilizzato in biochimica e biologia molecolare come substrato cromogenico nel dosaggio dell'attività dell'α-L-arabinofuranosidasi. Le α-L-arabinofuranosidasi sono enzimi che catalizzano l'idrolisi dei legami α-L-arabinofuranosidici, presenti in vari composti naturali, tra cui polisaccaridi e glicoconiugati. Questi enzimi svolgono un ruolo cruciale nella scomposizione e nel metabolismo dei carboidrati complessi, contribuendo alla degradazione della biomassa vegetale e al ciclo della materia organica nell'ambiente.
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6) Referenze
- Idrolasi glicosidiche bifunzionali della famiglia 3 dell'orzo con attività alfa-L-arabinofuranosidasi e beta-D-xilosidasi. Caratterizzazione, strutture primarie ed elaborazione COOH-terminale. | Lee, RC., et al. 2003. J Biol Chem. 278: 5377-87. PMID: 12464603
- Gli acetati di p-nitrofenile alfa-L-arabinofuranoside - preparazione regioselettiva per azione delle lipasi. | Mastihubová, M., et al. 2006. Bioorg Med Chem. 14: 1805-10. PMID: 16288881
- Variazione della specificità relativa del substrato della beta-D-xilosidasi/alfa-L-arabinofuranosidasi bifunzionale mediante mutazioni in un singolo sito: ruoli della distorsione e del riconoscimento del substrato. | Jordan, DB. and Li, XL. 2007. Biochim Biophys Acta. 1774: 1192-8. PMID: 17689155
- Costruzione e caratterizzazione di due enzimi chimerici per la degradazione dello xilano. | Fan, Z., et al. 2009. Biotechnol Bioeng. 102: 684-92. PMID: 18828173
- Termodinamica delle reazioni di idrolisi di acetato di 1-naftile, acetato di 4-nitrofenile e 4-nitrofenil α-L-arabinofuranoside. | Decker, SR., et al. 2010. J Phys Chem B. 114: 16060-7. PMID: 20361764
- Nuova alfa-L-arabinofuranosidasi/xylobioidrolasi bifunzionale (ABF3) da Penicillium purpurogenum. | Ravanal, MC., et al. 2010. Appl Environ Microbiol. 76: 5247-53. PMID: 20562284
- Azione degli enzimi deacetilanti dello xilano sui derivati monoacetilici dei glicosidi 4-nitrofenilici del β-D-xilopiranosio e dell'α-L-arabinofuranosio. | Biely, P., et al. 2011. J Biotechnol. 151: 137-42. PMID: 21029756
- Purificazione e caratterizzazione dell'arabinofuranosidasi dell'endofita del mais Acremonium zeae. | Bischoff, KM., et al. 2011. Biotechnol Lett. 33: 2013-8. PMID: 21671092
- L'analisi della famiglia di geni dell'arabinoxilano arabinofuranoidrolasi nell'orzo non supporta il loro coinvolgimento nel rimodellamento delle pareti cellulari dell'endosperma durante lo sviluppo. | Laidlaw, HK., et al. 2012. J Exp Bot. 63: 3031-45. PMID: 22378943
- Attivazione con metalli divalenti di una β-xilosidasi GH43. | Lee, CC., et al. 2013. Enzyme Microb Technol. 52: 84-90. PMID: 23273276
- Una nuova eso-α-l-arabinofuranosidasi/endo-xilanasi bifunzionale GH51 da Alicyclobacillus sp. A4 con una significativa capacità di degradazione della biomassa. | Yang, W., et al. 2015. Biotechnol Biofuels. 8: 197. PMID: 26628911
- Caratterizzazione di un'arabinofuranosidasi putativa della famiglia 43 delle glicosidi idrolasi di Aspergillus niger e suo potenziale utilizzo nella produzione di birra. | Li, X., et al. 2020. Food Chem. 305: 125382. PMID: 31525590
- Caratterizzazione e analisi funzionale di due nuove α-L-arabinofuranosidasi termotolleranti appartenenti alla famiglia delle glicosido idrolasi 51 di Thielavia terrestris e alla famiglia 62 di Eupenicillium parvum. | Long, L., et al. 2020. Appl Microbiol Biotechnol. 104: 8719-8733. PMID: 32880690
- La beta-D-xilosidasi di Trichoderma reesei è una beta-D-xilan xilidrolasi multifunzionale. | Herrmann, MC., et al. 1997. Biochem J. 321 (Pt 2): 375-81. PMID: 9020869
- Purificazione e caratterizzazione di una nuova alfa-L-arabinofuranosidasi termostabile da un ceppo variabile di Aureobasidium pullulans. | Saha, BC. and Bothast, RJ. 1998. Appl Environ Microbiol. 64: 216-20. PMID: 9435077
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
4-Nitrophenyl α-L-arabinofuranoside, 10 mg | sc-220982 | 10 mg | $109.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 25 mg | sc-220982A | 25 mg | $203.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 50 mg | sc-220982B | 50 mg | $359.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 100 mg | sc-220982C | 100 mg | $515.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 250 mg | sc-220982D | 250 mg | $983.00 |
