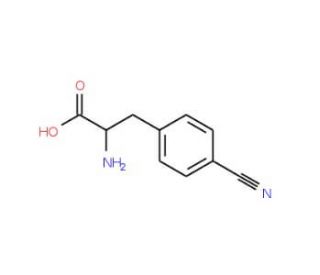
4-Cyano-L-phenylalanine (CAS 104531-20-6)
LINK RAPIDI
La 4-ciano-L-fenilalanina è un derivato dell'amminoacido e appartiene alla classe degli amminoacidi aromatici. La 4-ciano-L-fenilalanina è caratterizzata dalla presenza di un gruppo ciano (CN) attaccato alla molecola di fenilalanina. Nella ricerca scientifica, la 4-ciano-L-fenilalanina trova diverse applicazioni grazie alle sue proprietà chimiche uniche. Viene comunemente utilizzata come elemento costitutivo o precursore nella sintesi di peptidi e nella scoperta di farmaci. Il gruppo ciano può fungere da gruppo funzionale versatile, consentendo l'introduzione di diverse modifiche chimiche e la creazione di analoghi peptidici con attività biologiche alterate. Una delle applicazioni principali della 4-ciano-L-fenilalanina è nel campo della chimica medicinale. I ricercatori utilizzano questo composto per sviluppare nuovi peptidi con maggiore bioattività, stabilità o proprietà farmacocinetiche. Incorporando la 4-ciano-L-fenilalanina nelle sequenze peptidiche, gli scienziati possono modulare le interazioni del peptide con i bersagli biologici, come recettori o enzimi, portando potenzialmente a una maggiore efficacia terapeutica. Il meccanismo d'azione della 4-ciano-L-fenilalanina dipende dal contesto specifico e dal peptide o dalla molecola in cui viene incorporata. Come derivato aminoacidico, la 4-Ciano-L-fenilalanina può partecipare alla formazione del legame peptidico durante la sintesi, contribuendo alla struttura e alla funzione complessiva del peptide risultante. La presenza del gruppo ciano può influenzare le interazioni del peptide con i bersagli biologici, alterandone la conformazione, la stabilità o l'affinità di legame con i recettori. Inoltre, il gruppo ciano può subire reazioni chimiche, consentendo ulteriori modifiche o funzionalizzazioni del peptide. Queste modifiche possono avere un impatto sulla solubilità, sulla permeabilità di membrana o sulla stabilità metabolica del peptide, influenzandone il comportamento nei sistemi biologici.
4-Cyano-L-phenylalanine (CAS 104531-20-6) Referenze
- Nuovi substrati cromogenici della catepsina G neutrofila umana contenenti residui aminoacidici aromatici non naturali in posizione P(1) selezionati con metodi di chimica combinatoria. | Wysocka, M., et al. 2007. Mol Divers. 11: 93-9. PMID: 17653609
- Espansione dell'utilità della 4-ciano-L-fenilalanina come reporter vibrazionale degli ambienti proteici. | Bazewicz, CG., et al. 2012. J Phys Chem B. 116: 10824-31. PMID: 22909326
- Progettazione razionale di una proteina legante la ftalocianina di zinco. | Mutter, AC., et al. 2014. J Struct Biol. 185: 178-85. PMID: 23827257
- Sonda vibrazionale sensibile, sito-specifica e stabile degli ambienti locali delle proteine: 4-azidometil-L-fenilalanina. | Bazewicz, CG., et al. 2013. J Phys Chem B. 117: 8987-93. PMID: 23865850
- Il ruolo di 'guardiano' di Trp222 determina l'enantiopreferenza della dichetoreduttasi verso il 2-cloro-1-feniletanone. | Ma, H., et al. 2014. PLoS One. 9: e103792. PMID: 25072248
- Isolamento e diversificazione sintetica della jadomicina 4-amino-l-fenilalanina. | Martinez-Farina, CF., et al. 2015. J Nat Prod. 78: 1208-14. PMID: 26035093
- Miglioramento dell'incorporazione di amminoacidi non canonici da parte di un tRNA(Tyr) soppressore ingegnerizzato. | Rauch, BJ., et al. 2016. Biochemistry. 55: 618-28. PMID: 26694948
- Sperimentazione dell'efficacia del reporter spettroscopico di aminoacidi innaturali: uno studio strutturale. | Dippel, AB., et al. 2016. Acta Crystallogr D Struct Biol. 72: 121-30. PMID: 26894540
- Confronto tra cromofori biologici: proprietà fotofisiche dei derivati della cianofenilalanina. | Martin, JP., et al. 2016. Phys Chem Chem Phys. 18: 20750-7. PMID: 27412819
- Sonde minimaliste di IR e fluorescenza della funzione delle proteine. | Gosavi, PM. and Korendovych, IV. 2016. Curr Opin Chem Biol. 34: 103-109. PMID: 27599185
- Esplorazione degli ambienti locali di solvatazione di una proteina eme utilizzando il reporter spettroscopico 4-ciano-l-fenilalanina. | Kearney, C., et al. 2018. RSC Adv. 8: 13503-13512. PMID: 29780583
- Strutture di cristallo della proteina verde fluorescente con l'amminoacido innaturale 4-nitro-L-fenilalanina. | Maurici, N., et al. 2018. Acta Crystallogr F Struct Biol Commun. 74: 650-655. PMID: 30279317
- Indagine strutturale e spettrofotometrica di due cromofori innaturali alterati da amminoacidi nella proteina fluorescente verde superfolder. | Olenginski, GM., et al. 2021. Acta Crystallogr D Struct Biol. 77: 1010-1018. PMID: 34342274
- Peptidi progettati ex novo per il rilascio cellulare e la localizzazione subcellulare. | Rhys, GG., et al. 2022. Nat Chem Biol. 18: 999-1004. PMID: 35836017
- Svelare i complessi ambienti locali delle proteine con la 4-ciano-l-fenilalanina. | Lee, B., et al. 2022. J Phys Chem B. 126: 8957-8969. PMID: 36317866
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
4-Cyano-L-phenylalanine, 1 g | sc-290253 | 1 g | $156.00 | |||
4-Cyano-L-phenylalanine, 5 g | sc-290253A | 5 g | $604.00 |
