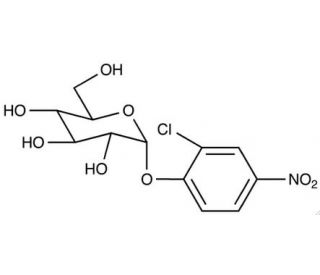
2-Chloro-4-nitrophenyl-α-D-glucopyranoside 의 분자 구조, CAS 번호: 119047-14-2
2-Chloro-4-nitrophenyl-α-D-glucopyranoside (CAS 119047-14-2)
대체 이름:
CNP-α-D-glucopyranoside
적용:
2-Chloro-4-nitrophenyl-α-D-glucopyranoside 는 CNP와 α-D- 포도당 사이의 결합을 표적으로 하는 효소를 위한 발색 기질입니다.
CAS 등록번호:
119047-14-2
순도:
≥98%
분자량:
335.69
분자식:
C12H14ClNO8
연구용으로만 사용가능합니다. 진단이나 치료용으로 사용불가합니다.
* Refer to Certificate of Analysis for lot specific data.
빠른 링크
주문정보
설명
기술정보
안전정보
SDS 및 분석 증명서
2-클로로-4-니트로페닐-α-D-글루코피라노사이드는 화학적으로 합성된 배당체로 생화학 연구, 특히 글리코시다제와 관련된 효소 활성 연구에서 중요한 도구로 사용됩니다. 이 화합물은 특정 글리코시다아제에 의한 효소 절단 시 2-클로로-4-니트로페놀 모이티를 방출하도록 설계되어 효소 동역학 및 특이성을 측정하는 데 탁월한 기질입니다. 방향족 고리의 클로로 및 니트로 그룹은 전자 인출 능력을 향상시켜 효소 절단 속도에 큰 영향을 미치므로 이러한 효소의 작용 메커니즘에 대한 통찰력을 제공합니다. 이 배당체는 다양한 조건에서 글리코시다제의 활성을 특성화하여 탄수화물 대사에서의 역할을 더 깊이 이해하는 데 도움이 됩니다. 2-클로로-4-니트로페닐-α-D-글루코피라노사이드는 포도당 중합체의 α-결합에 대한 특이성으로 인해 세포 생물학 및 생화학의 기본인 복합 탄수화물 분해와 관련된 연구에 특히 유용합니다. 이 연구 도구를 통해 과학자들은 글리코시다아제의 기질 선호도와 동역학적 거동을 조사할 수 있어 이러한 효소에 대한 지식을 발전시킬 수 있습니다. 이러한 응용 분야는 기초 과학 연구에서 화합물의 가치와 생화학 경로 및 분자 상호 작용에 대한 이해를 높이는 데 있어 화합물의 역할을 강조합니다.
2-Chloro-4-nitrophenyl-α-D-glucopyranoside (CAS 119047-14-2) 참고자료
- 보리 알파-아밀라아제 1의 단일 및 이중 서브사이트 +1/+2 및 -5/-6의 돌연변이에 의한 활성 및 기질 결합 모드의 조절. | Mori, H., et al. 2001. Eur J Biochem. 268: 6545-58. PMID: 11737209
- 글리코실 트랜스퍼라제 촉매 당 뉴클레오타이드 합성의 범위 확대. | Gantt, RW., et al. 2013. Proc Natl Acad Sci U S A. 110: 7648-53. PMID: 23610417
- GH97 반전 글리코사이드 가수분해 효소에서 칼슘 이온의 촉매 역할. | Okuyama, M., et al. 2014. FEBS Lett. 588: 3213-7. PMID: 25017438
- 수용액에서 에피메릭 배당체와 α- 및 β- 배당체 결합을 구별하는 이핵 구리(II) 착물. | Striegler, S., et al. 2016. J Catal. 338: 349-364. PMID: 27667854
- 2-클로로-4-니트로페닐-N-아세틸-베타-D-글루코사미네이드를 기질로 사용한 요로 N-아세틸-베타-D-글루코사미니다아제의 동역학 속도 분석. | Makise, J., et al. 1988. Clin Chem. 34: 2140-3. PMID: 3255304
- 말토오스에서 C7/C8-사이클리톨 및 C7N-아미노사이클리톨의 합성 및 아밀로스타틴 GXG 유사 유도체와 복합체에서 스트렙토마이세스 코엘리컬러 GlgEI V279S의 X-선 결정 구조. | Thanvi, R., et al. 2022. Front Chem. 10: 950433. PMID: 36157042
- 보리 알파-아밀라아제 1의 촉매 (베타/알파) 8-배럴 도메인에 기질 결합에 관여하는 네 번째 베타-알파 루프에서 무작위 돌연변이 유발을 통해 향상된 활성 및 조절된 작용 패턴을 얻었습니다. | Matsui, I. and Svensson, B. 1997. J Biol Chem. 272: 22456-63. PMID: 9278396
주문정보
| 제품명 | 카탈로그 번호 | 단위 | 가격 | 수량 | 관심품목 | |
2-Chloro-4-nitrophenyl-α-D-glucopyranoside, 100 mg | sc-220716 | 100 mg | $320.00 |
