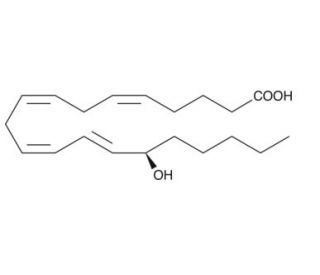
15(R)-HETE (CAS 83603-31-0)
LINK RAPIDI
Il 15(R)-HETE, con numero CAS 83603-31-0, è un enantiomero dell'acido 15-idrossieicosatetraenoico, che si distingue specificamente per la configurazione R del gruppo ossidrilico al quindicesimo carbonio della catena eicosanoide. Questo composto viene sintetizzato attraverso l'azione della 15-lipossigenasi sull'acido arachidonico. Nell'ambito della ricerca biochimica, il 15(R)-HETE è particolarmente apprezzato per il suo ruolo nel chiarire i meccanismi alla base della regolazione di processi cellulari come l'infiammazione, la segnalazione cellulare e la modulazione dei canali ionici. Le azioni specifiche del 15(R)-HETE comprendono l'influenza sul comportamento di varie vie di segnalazione critiche per la sopravvivenza, la differenziazione e la risposta allo stress ossidativo delle cellule. I ricercatori utilizzano questo composto per studiare i suoi effetti sui livelli di calcio intracellulare e la sua interazione con specifici recettori e proteine coinvolti nella trasduzione del segnale. Questa attenzione aiuta a svelare le complesse interazioni tra mediatori lipidici e meccanismi cellulari, migliorando la comprensione di come la segnalazione lipidica contribuisca alla regolazione dei processi fisiologici. Indagando i ruoli funzionali del 15(R)-HETE, gli scienziati acquisiscono conoscenze sulle interazioni molecolari dettagliate che regolano le risposte e gli adattamenti cellulari, contribuendo in modo significativo al campo più ampio della biologia cellulare e molecolare.
15(R)-HETE (CAS 83603-31-0) Referenze
- 15-Lipossigenasi nell'infiammazione glomerulare. | Montero, A. and Badr, KF. 2000. Exp Nephrol. 8: 14-9. PMID: 10644878
- Requisiti spaziali per la sintesi dell'acido 15-(R)-idrossi-5Z,8Z,11Z, 13E-eicosatetraenoico all'interno del sito attivo della ciclossigenasi della COX-2 murina. Perché la COX-1 acetilata non sintetizza il 15-(R)-etere. | Rowlinson, SW., et al. 2000. J Biol Chem. 275: 6586-91. PMID: 10692466
- Mediatori antinfiammatori endogeni dell'arachidonato nei neutrofili umani. | Vachier, I., et al. 2002. Biochem Biophys Res Commun. 290: 219-24. PMID: 11779156
- Danno al DNA mediato dalla ciclossigenasi-2. | Lee, SH., et al. 2005. J Biol Chem. 280: 28337-46. PMID: 15964853
- La 15-epi-lipossina A4 attivata dall'aspirina predice la ciclossigenasi-2 nei polmoni di topi trattati con LPS, ma non nella circolazione: implicazioni per un test clinico. | Kirkby, NS., et al. 2013. FASEB J. 27: 3938-46. PMID: 23792301
- Aspirina e mediatori lipidici nel sistema cardiovascolare. | Schrör, K. and Rauch, BH. 2015. Prostaglandins Other Lipid Mediat. 121: 17-23. PMID: 26201059
- Analisi degli HETE nel sangue intero umano mediante UHPLC-ECAPCI/HRMS chirale. | Mazaleuskaya, LL., et al. 2018. J Lipid Res. 59: 564-575. PMID: 29301865
- L'attività ciclossigenasi residua della COX-2 acetilata dall'aspirina forma 15 R-prostaglandine che inibiscono l'aggregazione piastrinica. | Giménez-Bastida, JA., et al. 2019. FASEB J. 33: 1033-1041. PMID: 30096040
- Caratterizzazione di specifici siti subcellulari di legame dell'acido 15-idrossieicosatetraenoico (15-HETE) su cellule di leucemia basofila di ratto. | Kang, LT. and Vanderhoek, JY. 1995. Biochim Biophys Acta. 1256: 297-304. PMID: 7786891
- La mutazione della serina-516 nella prostaglandina G/H sintasi-2 umana in metionina o l'acetilazione con aspirina di questo residuo stimola la sintesi di 15-R-HETE. | Mancini, JA., et al. 1994. FEBS Lett. 342: 33-7. PMID: 8143845
Informazioni ordini
| Nome del prodotto | Codice del prodotto | UNITÀ | Prezzo | Quantità | Preferiti | |
15(R)-HETE, 25 µg | sc-205032 | 25 µg | $139.00 | |||
15(R)-HETE, 50 µg | sc-205032A | 50 µg | $199.00 |
